Koordination:
M. Klimpfinger, Graz
Unter Mitarbeit von:
G. Mikus, Innsbruck
A. Reiner, Wien
F. Wrba, Wien
Problemstellung
Die pathologische Klassifikation von Magenkarzinomen ist essentiell für die Primärdiagnose, die Wahl des chirurgischen Therapieverfahrens und die Prognosebeurteilung. Dabei ist die genaue Lokalisationsangabe des Primärtumors entsprechend der anatomischen Magenregion ebenso wichtig wie die Kenntnis der makroskopischen Wachstumstypen, die für die Entnahme des Biopsiematerials bedeutungsvoll ist. Neben der histologischen Dignitätsdiagnose liefert die histologische Klassifikation nach Laurén präoperativ eine wesentliche Entscheidungshilfe für die Wahl des chirurgischen Therapieverfahrens. Zusammen mit der Primärtumorlokalisation beeinflußt der histologische Laurén-Typ die Entscheidung Gastrektomie versus distaler Resektion entscheidend, da der intestinale Typ nach Laurén mit geringeren Sicherheitsabständen als der diffuse Typ reseziert werden kann. Die Gefrierschnittuntersuchung ist intraoperativ hilfreich, um die Tumorfreiheit von chirurgischen Resektionsflächen histologisch abzusichern. Postoperativ ist die pathologische Klassifikation essentiell für die Prognosebeurteilung und wird in Zukunft darüberhinaus eine entscheidende Rolle bei der Wahl adjuvanter Tumortherapieverfahren spielen. Die Residualtumorklassifikation der UICC ermöglicht die Unterscheidung von potentiell kurativen (R-0-) und primär palliativen Eingriffen (R-1-, R-2-Resektionen). Das Tumorstaging der UICC mit den Tumorstadien 0-IV ist für eine differenzierte Prognosebeurteilung wesentlich, vor allem innerhalb der Gruppe der R-0-resezierten Patienten.
Ziel
Das wesentlichste Ziel der pathologischen Klassifikation von Magenkarzinomen ist es, zu einer differenzierten histologie- und stadiengerechten Tumortherapie beizutragen. Die Diagnostik und Therapie von Magenkarzinomen erfolgt zunehmend in multidisziplinärer Kooperation von Gastroenterologen, Radiologen, Pathologen, Chirurgen, internistischen Onkologen und Strahlentherapeuten. In diesem Zusammenhang ist hervorzuheben, daß ein klinisch-orientierter Pathologe in dieses Team integriert werden muß. Dies ist heute im Rahmen der interdisziplinären Qualitätssicherung im Sinne des Patienten unerläßlich.
Einleitung
Trotz der Abnahme der Inzidenz stellt das Magenkarzinom immer noch eine der wichtigsten Karzinomtodesursachen dar. Die Prognose beim Magenkarzinompatienten ist wesentlich von der Tumorausbreitung abhängig. Nur durch eine verbesserte Früherkennung einerseits und eine konsequente histologie- und stadiengerechte chirurgische Therapie andererseits kann die Prognose bei Magenkarzinompatienten weiter verbessert werden. Die Primärtumorlokalisation, der makroskopische Wachstumstyp und die histologische Klassifikation von Magenkarzinomen spielen sowohl für die Diagnosesicherung und Wahl des chirurgischen Behandlungsverfahrens, als auch für die Prognosebeurteilung und in der Zukunft auch für die Entscheidung der Wahl adjuvanter Therapieverfahren eine wesentliche Rolle.
Lokalisation und Makroskopie
Nach den Regeln der UICC werden hinsichtlich der Tumorlokalisation die anatomischen Abschnitte Kardia, Fundus, Korpus, Antrum und Pylorus unterschieden. Bei der Tumorinfiltration mehrerer dieser Regionen ist der Tumor primär der Region mit der größten Tumormasse zuzuordnen. Eine möglichst präzise Lokalisationsangabe des Primärtumors durch den Endoskopiker ist wesentlich für die Wahl des chirurgischen Behandlungsverfahrens.
Die Kenntnis der makroskopischen Wachstumstypen nach Borrmann I-IV (Tab. 1) ist für die gezielte Entnahme von Biopsiematerial außerordentlich wichtig und erlaubt zudem eine grobe Vorbeurteilung der Tumorausdehnung. Bei der Entnahme von Biopsiematerial müssen reichlich Proben sowohl vom Rand als auch vom Grund der makroskopisch erkennbaren Läsion entnommen werden (mindestens 6, in der Regel zwischen 6 und 12 Biopsien), um einerseits eine repräsentative Dignitätsdiagnose stellen und darüber hinaus eine differenzierte histologische Tumorklassifikation durchführen zu können.
Tab. 1: Makroskopische Typen nach Borrmann I-IV
| I. | Vorwiegend exophytisch wachsen- de, meist breitbasig polypöse Karzinome |
| II. | Karzinome mit zentraler Ulzeration mit steilen wallartig aufgeworfenen Rändern und relativ scharfer Abgrenzung zur Umgebung. |
| III. | Karzinome mit zentraler Exulzeration ohne wallartig aufge- worfene Ränder und mit unscharfer Abgrenzungen zur Umgebung |
| IV. | Diffuse Tumorinfiltration der Magenwand |
Histologische Klassifikation
Die präoperativ im Biopsiematerial durchführbare Laurén-Klassifikation ist vor allem für das Ausmaß der Operation aufgrund verschiedener Sicherheitsabstände vom Tumorrand beim diffusen, bzw. intestinalen Typ bedeutungsvoll und beeinflußt damit zusammen mit der Primärtumorlokalisation entscheidend die Wahl des chirurgischen Therapieverfahrens. Die konventionelle histologische Klassifikation nach WHO und das histopathologische Grading sollen zusätzlich zur Laurén-Klassifikation angegeben werden, wobei ihnen allerdings nur in Einzelfällen eine zusätzliche praktisch-prognostische Bedeutung zukommt.
Laurén-Klassifikation
- Intestinaler Typ
Das Tumorgewebe ist relativ scharf gegenüber der Umgebung abgegrenzt und zeigt meist tubuläre Tumorformationen, die von Zylinderepithel mit intestinalen Charakteristika ausgekleidet werden. Aufgrund dieser relativ guten Abgrenzung gegen die Umgebung sind beim intestinalen Typ geringere Mindestresektionsabstände vom makroskopisch erkennbaren Tumorrand erforderlich. In situ soll ein Sicherheitsabstand von 4-6 cm vom Tumorrand angestrebt werden, was am nicht ausgespannten, unfixierten Operationspräparat 2-3 cm entspricht. Bei der Messung der Resektionsabstände durch den Pathologen am fixierten, nicht ausgespannten Operationspräparat ist zusätzlich eine weitere fixationsbedingte Schrumpfung des Gewebes von 20-30% einzuberechnen, was dann in etwa 1,5-2 cm entspricht. Es ist in diesem Zusammenhang hervorzuheben, daß es wichtig ist, diese Meßbedingungen zu kennen und zu berücksichtigen, um klinisch-pathologische Mißverständnisse zu vermeiden. Weiters finden sich in der Nachbarschaft von Magenkarzinomen des intestinalen Typs signifikant gehäuft Dysplasien als sogenannte Ausläuferläsionen. Bei der histologischen Diagnose einer Dysplasie (verschiedener Grade) ist es seitens des Klinikers daher praktisch wichtig sicherzustellen, ob es sich um eine sogenannte Ausläuferläsion im Randbereich eines Karzinoms handelt, oder ob die Dysplasie per se die Läsion meist als sogenanntes flaches Adenom darstellt. Weiters finden sich in der Nachbarschaft von Magenkarzinomen des intestinalen Typs auch signifikant gehäuft schwere Formen der chronisch atrophen Gastritis mit verschiedenen Formen der intestinalen Metaplasie (vor allem Typ III der Sydney-Klassifikation), auf deren Basis die Karzinome vom intestinalen Typ entstehen. - Diffuser Typ
Die Abgrenzung des Tumorgewebes gegenüber dem nicht-neoplastischen Gewebe ist völlig unscharf, das Tumorgewebe kann sich über mehrere cm weit unter makroskopisch unverdächtiger Mukosa ausbreiten. Auch die Tiefeninfiltration ist makroskopisch und histologisch unscharf gegen das nicht-neoplastische Gewebe. Diese diffuse Tumorausbreitung ist histologisch in einer herabgesetzten Kohärenz der Tumorzellen untereinander begründet, wobei die Tumorzellen oft einzeln oder in kleinen Gruppen und Strängen diffus das umgebende nicht-neoplastische Gewebe infiltrieren. Tubuläre Strukturen sind in der Regel spärlich ausgebildet. Aufgrund der unscharfen Tumorabgrenzung und z. T. diffusen Tumorausbreitung unter makroskopisch unauffälliger Schleimhaut ergibt sich die Notwendigkeit weiterer Sicherheitsabstände vom Tumorrand, wobei 8-10 cm Sicherheitsabstand in situ anzustreben sind (entspricht wiederum am unfixierten, nicht ausgespannten Operationspräparat 4-5 cm und am fixierten, nicht ausgespannten Resektat etwa 2,5-3,5 cm).
Die Laurén-Klassifikation ist im Biopsiematerial durchführbar, die Diagnose im Biopsiematerial stimmt mit der Klassifikation im Resektat in ca. 90% der Fälle überein. Eine Fehlerquote von ca. 10% erklärt sich aus dem Vorkommen eines intestinalen Tumortyps an der Tumoroberfläche, während in der Tiefe bereits ein diffuser Karzinomtyp vorliegen kann. Ein Prozentsatz von etwa 10% diskrepanter Befunde spricht daher in der Praxis nicht gegen die Qualität der pathologischen Befunde, sondern durchaus für die Genauigkeit der pathohistologischen Aufarbeitung. Die präoperativ am Biopsiematerial durchführbare Klassifikation nach Laurén ist trotz einer unumgänglichen Fehlerrate von ca. 10% wesentlich für das Konzept einer differenzierten Tumortherapie bei Magenkarzinompatienten. In der Praxis sind auf dieser Basis durchschnittlich in etwa 2/3 der Fälle Gastrektomien und in 1/3 der Fälle subtotale aborale Resektionen erforderlich.
Auf die konventionelle histologische Klassifikation der WHO und das Tumorgrading soll hier aufgrund relativ geringer praktischer Bedeutung nicht näher eingegangen werden. Prinzipiell wird der Malignitätsgrad der Tumoren teilweise bereits mit dem histologischen Typing nach Laurén miterfaßt.
Tumorstaging
Für das Tumorstaging ist heute die parallele Durchführung der Residualtumorklassifikation und der Tumorstadienermittlung nach dem TNM-System (Tab. 2a, b) der UICC als unerläßlicher Standard anzusehen.
| Tabelle 2a) | Definition der TNM-Kategorien |
| T | Primärtumor |
| TX | Primärtumor kann nicht beurteilt werden |
| T0 | Kein Anhalt für Primärtumor |
| Tis | Carcinoma in situ: intraepithelialer Tumor ohne Infiltration der Lamina propria |
| T1 | Tumor infiltriert Lamina propria oder Submukosa |
| T2 | Tumor infiltriert Muscularis propria oder Subserosa (1) |
| T3 | Tumor penetriert Serosa (viszerales Peritoneum), infiltriert aber nicht benachbarte Strukturen (1, 2, 3) |
| T4 | Tumor infiltriert benachbarte Strukturen (3, 4) |
| N | Regionäre Lymphknoten |
| NX | Regionäre Lymphknoten können nicht beurteilt werden |
| N0 | Keine regionären Lymphknotenmetastasen |
| N1 | Metastasen in perigastrischen Lymphknoten innerhalb 3 cm vom Rand des Primärtumors |
| N2 | Metastasen perigastrischer Lymphknoten weiter als 3 cm vom Rand des Primärtumors oder in Lymphknoten entlang der Aa. gastrica sinistra, hepatica communis, lienalis oder coeliaca (4) |
| M | Fernmetastasen |
| MX | Das Vorliegen von Fernmetastasen kann nicht beurteilt werden |
| M0 | Keine Fernmetastasen |
| M1 | Fernmetastasen |
| Interpretation: | |
| 1. | Eine Tumorausbreitung zwischen den Serosablättern und in das angrenzende Fettgewebe der Ligamente oder des großen oder kleinen Netzes ohne Perforation der Serosa ist als T2 zu klassifizieren |
| 2. | Benachbarte Strukturen sind Milz, Colon transversum, Leber, Zwerchfell, Pankreas, Bauchwand, Nebennieren, Dünndarm und Retroperitoneum |
| 3. | Intramurale Ausbreitung im Duodenum oder Ösophagus wird nach der tiefsten Infiltration in diesen Organen oder im Magen klassifiziert |
| 4. | Befall von anderen intraabdominalen Lymphknoten, wie hepato-duodenalen, retropankreatischen, mesenterialen oder paraaortalen Lymphknoten, gilt als Fernmetastasierung und ist mit pM 1 LYM zu klassifizieren |
| Tabelle 2 b) | Tumorstadien 0 bis IV nach UICC | ||
| Stadium 0 | Tis | N0 | M0 |
| Stadium IA | T1 | N0 | M0 |
| Stadium IB | T1 | N1 | M0 |
| T2 | N0 | M0 | |
| Stadium II | T1 | N2 | M0 |
| T2 | N1 | M0 | |
| T3 | N0 | M0 | |
| Stadium IIIA | T2 | N2 | M0 |
| T3 | N1 | M0 | |
| T4 | N0 | M0 | |
| Stadium IIIB | T3 | N2 | M0 |
| T4 | N1 | M0 | |
| Stadium IV | T4 | N2 | M0 |
| Jedes T | Jedes N | M1 | |
Die Residual (R)-Tumorklassifikation der UICC bezeichnet das Fehlen oder Vorhandensein von nachweisbarem Residualtumor (Resttumor) nach erfolgter Therapie und wird mit dem Symbol R beschrieben. R-0 bedeutet kein nachweisbarer Residualtumor, während R-1 einen mikroskopisch und R-2 einen makroskopisch nachweisbaren Residualtumor bezeichnen. Daher gelten nach den Regeln der UICC sowohl loko-regionärer Tumor als auch nicht resezierbare Fernmetastasen als Residualtumor. Die Residualtumorklassifikation soll bei Magenkarzinomen in jedem Fall durchgeführt werden, da primär palliative Eingriffe (R-1-, R-2-Resektion) von potentiell kurativen (R-0-Resektion) unterschieden werden können. Die Unterscheidung ist prognostisch statistisch höchst signifikant. Fälle, in denen die Residualtumorklassifikation nicht eindeutig möglich ist, sind mit R-X zu klassifizieren. An dieser Stelle ist hervorzuheben, daß die Residualtumorklassifikation eine enge klinisch-pathologische Zusammenarbeit erfordert. Seitens des Pathologen müssen bezüglich der Residualtumorklassifikation nicht nur der orale und aborale chirurgische Resektionsrand, sondern vor allem auch die Resektionsflächen im Bereich des Halteapparetes (kleines Netz, Ligamentum gastrocolicum, etc.) histologisch untersucht werden. Bei organüberschreitender Resektion sind die Resektionsflächen an mitresezierten Organen ebenfalls histologisch zu untersuchen.
Tumorstadien 0-IV nach UICC
Der Ermittlung der Tumorstadien 0-IV nach UICC kommt wesentliche prognostische Bedeutung zu. Vor allem bei den R-0-resezierten Fällen lassen sich auf der Basis dieses TNM-Stagings statistisch signifikante und prognostisch relevante Tumorstadien ermitteln. Dabei wird im TNM-System das Tumorstadium aus der Kombination der jeweiligen T-, N- und M-Kategorie ermittelt. Den klinischen T-, N- und M-Kategorien entsprechen die jeweiligen pathologischen Kategorien, die mit p als pT, pN oder pM zu kennzeichnen sind. Die T-Kategorie beschreibt jeweils die tiefste Tumorinfiltration des vorliegenden Tumors, die N-Kategorie die Tumorausbreitung im Bereich der regionären Lymphabflußgebiete und die M-Kategorie das Fehlen oder Vorhandensein von Fernmetastasen (siehe Tab. 2a, b). Seitens des Pathologen ist bei der histologischen Präparataufarbeitung vor allem auf den Serosadurchbruch, sowie auf eine repräsentative Anzahl histologisch untersuchter Lymphknoten zu achten. Für Gastrektomien sollte die Zahl durchschnittlich untersuchter histologisch verifizierter Lymphknoten zumindest zwischen 25 und 30, bei subtotalen aboralen Resektionen zwischen 15 und 20 liegen. Klassifikationen anhand von durchschnittlich weniger als 15 histologisch verifizierten Lymphknoten können unter Berücksichtigung heutiger Qualitätsstandards als nicht mehr ausreichend angesehen werden.
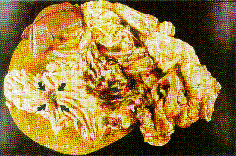

Abb. 1a und 1b:
Gastrektomiepräparat mit fortgeschrittenem Magenkarzinom vom makroskopischen Typ III nach Borrmann (Pfeile).
Spezielle Begriffe
- Magenfrühkarzinom
Das Magenfrühkarzinom ist durch die Beschränkung des neoplastischen Prozesses auf die Magenmukosa (Mukosatyp) oder auf die Mukosa und Submukosa (Submukosatyp) definiert, unabhängig von der Flächenausdehnung und unabhängig vom Lymphknotenstatus. Die Muscularis propria des Magens ist dabei tumorfrei, was nur nach kompletter histologischer Aufarbeitung des Tumors bewiesen werden kann. Die Diagnose Magenfrühkarzinom kann daher präoperativ im Biopsiematerial nur vermutet werden und muß im Operationspräparat verifiziert werden. Auch mittels Endosonographie ist die Diagnose Magenfrühkarzinom eine zwar häufig zutreffende, aber dennoch lediglich eine Vermutungsdiagnose. In Europa und USA liegt der Prozentsatz der Magenfrühkarzinome bezogen auf die Gesamtzahl operierter Magenkarzinompatienten zwischen 5 und 20%, in Japan zwischen 40 und 60% (hohe Inzidenz/flächendeckendes Screening-Programm). Für Europa und die USA gilt eine Magenfrühkarzinomrate von 20-25% als sehr guter Standard. Raten von weniger als 10% zeigen einen schlechten klinischen Standard in der Primärdiagnostik oder eine hohe Selektion im Rahmen der Patientenzuweisung an. Bei Magenfrühkarzinomen finden sich häufiger intestinale als diffuse Typen nach Laurén. Lymphknotenmetastasen sind beim Mukosatyp in etwa 2-10% und beim Submukosatyp in etwa 4-20% der Fälle nachweisbar. Magenfrühkarzinome erfordern daher prinzipiell ebenso wie fortgeschrittene Magenkarzinome eine radikale chirurgische Therapie mit konsequenter Lymphadenektomie. - Kardiakarzinom
Magenkarzinome am ösophago-gastralen Übergang werden als Kardiakarzinome bezeichnet und sind von isolierten Karzinomen des Fundus ventriculi ebenso abzugrenzen wie von ausgedehnten Karzinomen des Corpus ventriculi oder des gesamten Magens. Da es sich in allen Regionen prinzipiell um ähnliche histologische Tumortypen und Subtypen handelt, ist eine eindeutige Zuordnung der Primärtumorlokalisation rein histologisch vielfach nicht möglich. Der Tumor ist nach den Regeln der UICC der Region mit der größten makroskopisch feststellbaren Tumormasse zuzuordnen. Außer der Abgrenzung gegenüber den Magenkarzinomen anderer Primärlokalisationen ist das Kardiakarzinom weiters von den Adenokarzinomen des distalen Ösophagus (z.B. bei Barett-Ösophagus) abzugrenzen. Plattenepithelkarzinome im ösophago-gastralen Übergangsbereich sind praktisch immer als distale Ösophaguskarzinome aufzufassen. Die histologische Klassifikation der Kardiakarzinome folgt prinzipiell den oben angeführten allgemeinen Klassifikationsrichtlinien von Magenkarzinomen. Allerdings müssen die Kardiakarzinome von den Magenkarzinomen aus mehreren Gründen getrennt ausgewertet werden. Kardiakarzinome werden überdurchschnittlich häufig in fortgeschritteneren Tumorstadien operiert und die Prognose ist dementsprechend durchschnittlich noch schlechter als bei fortgeschrittenen Magenkarzinomen anderer Primärlokalisationen. Auch das operationstaktische Vorgehen entspricht den bei distalen Ösophaguskarzinomen angewandten Therapieverfahren.
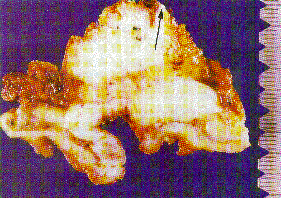
Abb. 2: Querschnitt durch ein fortgeschrittenes Magenkarzinom mit breiter und tiefer Infiltration des Fettgewebes an der kleinen Kurvatur mit Hineinreichen des Tumorgewebes an die chirurgische Resektionsfläche (Pfeile).
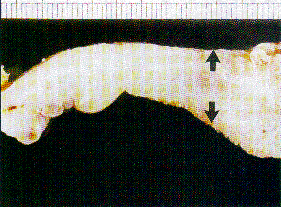
Abb. 3a: Makroskopischer Querschnitt durch ein fortgeschrittenes Magenkarzinom vom Typ IV nach Borrmann mit diffuser Infiltration der gesamten Magenwand (Pfeile).
Intraoperative Schnellschnittuntersuchung und Präparataufarbeitung für die Paraffinhistologie
Eine intraoperative Schnellschnittuntersuchung ist nur dann indiziert, wenn von der Diagnose das operationstaktische Vorgehen beeinflußt wird. Dies gilt vor allem für die Untersuchung von chirurgischen Resektionsrändern auf Tumorfreiheit (Vermeidung von R-1-Resektionen). Die histologische Verifikation einer diffusen Peritonealkarzinose sichert die Entscheidung zur Einschränkung des operativen Vorgehens auf einen Palliativeingriff ab. Für eine exakte makroskopische und histologische Aufarbeitung soll das Operationspräparat im Idealfall unmittelbar nach der Operation im nicht eröffneten Zustand dem Pathologen übergeben werden. Bei längerer Transportdauer soll das Präparat an der großen Kurvatur eröffnet und auf einer Korkplatte ausgespannt werden. Eine anschließende rasche Formolfixierung (10%iger gepufferter Formaldehyd) ist Voraussetzung für eine gute Qualität der pathologischen Aufarbeitung. Bei Verdacht auf Magenfrühkarzinom soll zusätzlich die Biopsiestelle am unfixierten Präparat fadenmarkiert werden, da die Auffindung solcher Bezirke am formolfixierten Präparat oft schwierig sein kann.
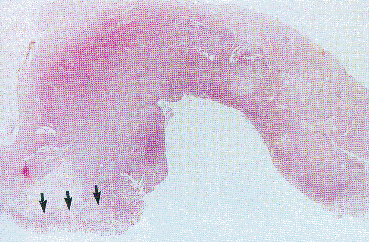
Abb. 3b: Histologischer Großflächenschnitt durch ein Magenkarzinom vom diffusen Typ nach Laurén mit Infiltration der gesamten Magenwand, sowie Unterminierung nicht-neoplastischer Magenschleimhaut durch Tumorgewebe (Pfeile).
Zusammenfassung
Die prä-, intra- und postoperativen pathologischen Befunde sind essentielle Bestandteile für die Diagnosesicherung, Wahl des chirurgischen Therapieverfahrens und die postoperative Prognosebeurteilung. Zukünftig werden diese außerdem eine wesentliche Rolle in der Wahl adjuvanter Therapieverfahren spielen. Es ist daher für die moderne multidisziplinäre Diagnostik und Therapie von Magenkarzinomen unerläßlich, daß ein klinisch-orientierter Pathologe in das Team von Gastroenterologen, Radiologen, Chirurgen, internistischen Onkologen und Strahlentherapeuten integriert wird.
