Koordination:
G.R. Jatzko, St. Veit
Unter Mitarbeit von:
R. Pointner, Zell a. See
H.J. Mischinger, Graz
G.P. Schwab, Innsbruck
R. Schiessel, Wien
H.R. Rosen, Wien
Ziel
Die radikale chirurgische Entfernung des Magenkarzinoms stellt zur Zeit die einzige Chance auf eine definitive Heilung dar. Abhängig von der Lokalisation sowie der Histologie des Tumors sind daher klare Standards bezüglich Resektionsausmaß und Lymphadenektomie zu fordern. Vor allem die prophylaktische Lymphknotenentfernung gemäß den Richtlinien der Japanese Research Society for Gastric Cancer ist in der Lage, eine wirkliche R-0-Radikalität und damit eine Überlebensverbesserung auch in den fortgeschritteneren Stadien II und IIIA (nach UICC) zu erreichen.
Operationsvorbereitung
Eine gute Operationsvorbereitung vermag Komplikationen und Letalität wesentlich zu senken. Bestandteil der Operationsvorbereitung sind die Korrektur von Hypo- und Dysproteinämien, der Ausgleich von Elektrolyt- und Flüssigkeitsdefiziten, von Anämien und Vitamindefiziten. Daneben gilt es, bestehende Organinsuffizienzen an Herz, Gefäßsystem, Lunge, Leber und Niere oder Stoffwechselstörungen (Diabetes, Niereninsuffizienz) zu beseitigen oder zu bessern. Vor allem bei Risikopatienten kommt der präoperativen, physiko- bzw. atemtherapeutischen Vorbereitung eine wesentliche Bedeutung zu.Bei einer Magenausgangstenose empfiehlt sich das Legen einer nasalen Magensonde, die parenterale Ernährung über einen zentralen Venenweg und unmittelbar präoperativ die Magenspülung bei intubierten Patienten. Eine optimale Reinigung des Dickdarmes ist präoperativ immer vorzunehmen (notwendige Erweiterung des Eingriffs bei Tumorinfiltration des Querkolons).
Lagerung des Patienten und operativer Zugang
Ein angemessen großzügiger Zugang belastet den Patienten wenig, beschleunigt den Eingriff und reduziert technische Schwierigkeiten. Für eine radikale Lymphadenektomie eignet sich am besten die mediane Laparotomie in Rückenlage, vom Xiphoid bis Mitte Unterbauch unter Umschneidung des Nabels links. Ein Bauchdeckenretraktor (Ringretraktor, Rochardhaken) ist unverzichtbar. Bei notwendiger Ausdehnung des Eingriffs auf den thorakalen Oesophagus muß die Möglichkeit der abdomino-linksthorakalen, transdiaphragmalen Inzisionserweiterung in halbschräger rechter Seitenlage gegeben sein. Auch das technische Equipment für eine zusätzliche posterolaterale rechte Thorakotomie muß vorhanden sein.
Resektion
C-Klassifikation
(Diagnosesicherungsgrad cTNM)
Die Verfeinerung diagnostischer Methoden wie CT, Sonographie, Endosonographie und präoperative Laparoskopie lassen gemeinsam mit der präoperativen Biopsiehistologie eine ungefähre Evaluation des Tumorstadiums zu (klinisches Staging). Dies erscheint besonders in Zusammenhang mit möglichen neoadjuvanten Therapiemodalitäten von Bedeutung. Intraoperativ ist eine möglichst genaue Evaluierung der Tumorausdehnung erforderlich und festzuhalten. Dies beinhaltet die Beschreibung der Tumorlokalisation und -ausdehnung, das Festhalten einer bestehenden Serosainfiltration und die Beurteilung der Tumorbeweglichkeit. Daneben ist die makroskopische Beurteilung einer erfolgten Metastasierung in regionale oder juxtaregionale Lymphknotenstationen, eine Peritonealkarzinose oder ein metastatischer Befall der Leber festzuhalten. Lebermetastasen sollten in jedem Fall histologisch verifiziert werden. Bei Serosainfiltration empfiehlt sich eine Abklatschzytologie (Objektträger) von der vermeintlich infiltrierten Magenwandstelle sowie eine Douglaszytologie aus vorhandenem Aszites oder aus einer Douglaslavage.
Kurative Resektion
Die vollständige Entfernung des Tumors bedeutet beim Magenkarzinom derzeit die einzige Chance auf Heilung. Die kurative Resektion umfaßt die Entfernung des tumortragenden Magenabschnittes weit im Gesunden einschließlich des großen und kleinen Netzes,die Entfernung des vorderen Blattes des Mesocolon Transversum und der Pankreaskapsel bei Tumorkontakt sowie die Dissektion der regionalen Lymphknoten und die Wiederherstellung der Passage. Ein zentrales Problem der kurativen Resektion betrifft die Festlegung der wahren Tumorgrenzen besonders in Bezug auf den Lymphknotenbefall , welche auch bei noch so exaktem präoperativen und intraoperativen Staging schwer abschätzbar ist. Daher ist die komplette lokoregionale Tumorentfernung mit adaequaten Sicherheitsabständen (R0-Resektion) der wichtigste Faktor in Bezug auf Lokalrezidiv- und Überlebensraten und kann ausschließlich durch eine möglichst radikale Lymphadenektomie erreicht werden.Die Entscheidung möglichst radikaler Eingriff, d.h . Gastrektomie mit radikaler D 2 Lymphknotendissektion (neue japanischeTerminologie, statt R1-R3 in Bezug auf das Ausmaß der Lymphknotendissektion) oder histologie-und stadiengerechte Chirurgie mit ausreichender Radikalität ist von verschiedenen klinischen und tumorbiologischen Faktoren abhängig. Diese Faktoren beinhalten die Laurén-Klassifikation, die Tumorlokalisation, die Infiltrationstiefe, eine mögliche Infiltration von Nachbarorganen, das Alter des Patienten und mögliche schwerwiegende Begleiterkrankungen.
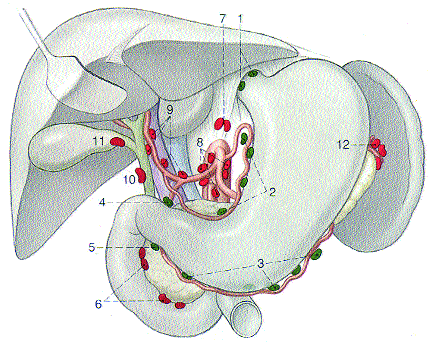
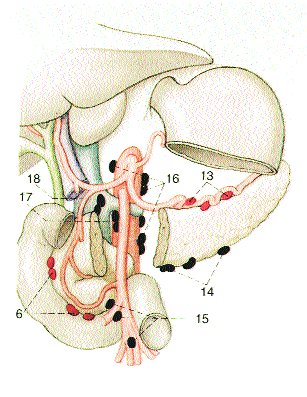
Einteilung der Lymphknotengruppen (nach: Japanese Research Society gastric cancer).
- Kompartment (grün): 1 Anulus lymphaticus cardiae, 2 Nodi lymphatici gastrici dextri et sinistri, 3 Nodi lymphatici gastro-epiploici dextri et sinistri,4 Nodi lymphatici suprapylorici, 5 Nodi lymphatici subpylorici et retropylorici.
- Kompartment (rot): 6 Nodi lymphatici pancreatico-duodenales superiores et inferiores, 7 Nodi lymphatici phrenici inferiores, 8 Nodi lymphatici coeliaci,9 Nodi lymphatici hepatici, 10 Nodi lymphatici foraminales, 11 Nodi lymphatici cystici, 12 Nodi lymphatici splenici, 13 Nodi lymphatici pancreaticisuperiores
- Kompartment (schwarz): 14 Nodi lymphatici pancreatici inferiores, 15 Nodi lymphatici mesenterici superiores, 16 Nodi lymphatici aortici laterales,17 Nodi lymphatici praeortici, 18 Nodi lymphatici praecavales
Resektionsausmaß
Bei der Bemessung des Sicherheitsabstandes muß die unterschiedliche, makroskopisch nicht sichtbare Ausbreitung der beiden histomorphologischen Typen des Magenkarzinoms (Laurén) berücksichtigt werden. Beim intestinalen Typ genügt ein proximaler Sicherheitsabstand von 4-6 cm in situ, während beim diffusen Typ ein proximaler Sicherheitsabstand von 8-10 cm gewählt werden muß. Der Mischtyp ist wie der diffuse Typ zu behandeln.Unter Berücksichtigung der Tumorlokalisation im unteren, mittleren oder oberen Magendrittel (A; M; C), des histologischen Typs und des einzuhaltenden Sicherheitsabstandes entsprechend der Laurén-Klassifikation, ergibt sich die chirurgische Entscheidung subtotale, distale Resektion oder Gastrektomie.
Die Gastrektomie stellt den Regeleingriff beim diffusen und multizentrischen Karzinom dar, ausgenommen kleine Karzinome im unteren Magendrittel ohne Serosainfiltration. Eine proximale Magenresektion ist bei kurativer Zielsetzung aus onkologischen und funktionellen Gründen abzulehnen.
Eine intraoperative Schnellschnittuntersuchung ist dann indiziert, wenn von der Diagnose das operationstaktische Vorgehen beeinflußt wird. Dies gilt vor allem für die Untersuchung des oralen chirurgischen Resektionsrandes auf Tumorfreiheit (Vermeidung von R1-Resektionen).
Die sogenannte proximale Resektion mit anschließender Ösophagoantrostomie als Rekonstruktion ist aus onkologischen wie auch aus funktionellen Gründen heute als obsolet abzulehnen.
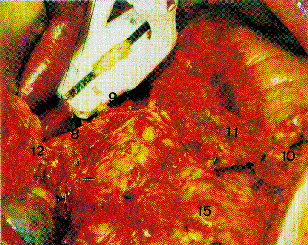
Zustand nach Gastrektomie und Lymphadenektomie der Kompartments I und II.
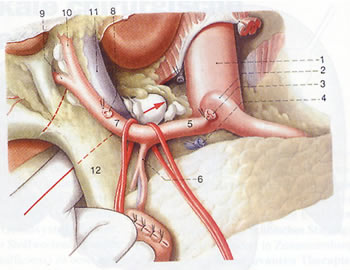
Die Arterien sind freigelegt. Man geht mit dem Zeigefinger der linken Hand (Pfeil) durch das Foramen Winslow, drückt die der Pfortader anliegenden Lymphknotengruppen nach oben heraus; sie werden mit Klemmen gefaßt und radikal exstirpiert.
- Pars abdominalis aortae
- Truncus coeliacus
- Stumpf der A. gastrica sinistra
- Stumpf der V. gastrica sinistra
- A. hepatica communis
- A. gastroduodenalis
- A. hepatica propria
- Stumpf der A. gastrica dextra
- A. hepatica propria dextra
- A. hepatica propria sinistra
- V. portae
- Ductus choledochus
Splenektomie
Die Indikation zur Splenektomie ergibt sich zwangsläufig, wenn die Lymphknoten des Milzhilus und die entlang der A.lienalis (Lymphknotenstationen 10 u. 11) zu entfernen sind.
Der Befall dieser Lymphknotenstationen ist abhängig von der Tumorlokalisation, vom histologischen Tumortyp, vom Wachstumstyp und von der Infiltrationstiefe. Beim Tumorsitz im unteren Magendrittel ist der Befall dieser Lymphknoten äußerst selten. Im allgemeinen ist mit der Indikation zur Gastrektomie auch die Indikation zur Zonensplenektomie gegeben. Die distale Pankreasresektion in Zusammenhang mit der Lymphadenektomie und Splenektomie hat sich wegen der dabei häufig auftretenden Komplikationen nicht bewährt. Die Lymphknotenstation 11 kann bei geplanter Splenektomie nach Mobilisierung von Milz und Pankreas einfach entfernt werden, indem sie en bloc mit der A.lienalis, nach Ligatur etwa 2 cm nach ihrem Abgang, entfernt wird (Maruyama Manöver).
Radikale Lymphadenektomiebeim Magenkarzinom
Die prophylaktische regionäre Lymphadenektomie ist ein zu forderndes Grundprinzip onkologischer Chirurgie, einmal wegen des nur dann möglichen Staging zum anderen aus Gründen der Radikalität. Die von japanischer Seite in den letzten 30 Jahren auf Grund chirurgisch-pathologischer Studien ausgearbeitete Lymphknotendissektion potentiell befallener regionärer Lymphknotenstraßen kann heute als standardisiertes Verfahren angesehen werden (Japanese Research Society for Gastric Cancer 1981).
Pathologische Anatomie der Lymphabflu ßbahnen
Am Magen bestehen prinzipiell 3 Lymphabflußzonen welche den Versorgungsgebieten der 3 großen Gefäße des Truncus, nämlich der A. gastrica sinistra, A. hepatica communis und A. lienalis entsprechen, sich aber weit überschneiden.Tumoren an der kleinen Kurvatur drainieren entlang der A. gastrica sinistra, Tumoren an der Kardia oder des Fundus zusätzlich über die A.lienalis und Tumoren im Corpusbereich großkurvaturseitig oder im Antrum über die A. gastroepiploica dextra und A. hepatica communis.
Damit ist je nach Tumorlage die Zielrichtung der Lymphknotendissektion festgelegt.
Einteilung der region ären Lymphknotengruppen (Abb.)
Die perigastrischen Lymphknoten (Lymphknoten der ersten Station) liegen der Magenwand unmittelbar an und werden in die Lymphknotengruppen 1-6 unterteilt.
Die Lymphknoten der zweiten Station liegen entlang der großen Gefäße und umfaßen die Gruppen 7-11. Noch tumorfernere Lymphknoten (dritte Station) umfaßen die Gruppe 12 (A. hepatica propria), 13 (retropankreatisch, retroduodenal), 14 (um den Stamm der A.mesenterica sup.), 15 (A.colica media), 16 (paraaortale Lymphknoten) und 110, 111 (paraoesophageale Lymphknoten). D1-Dissektion bedeutet die Entfernung der Gruppen 1-6 bei der Gastrektomie oder 3-6 bei der subtotalen Gastrektomie.
D2-Dissektion bedeutet die zusätzliche Entfernung der Gruppen 7-11 bei der Gastrektomie, 7-9 bei der subtotalen Gastrektomie. Bei der D3-Dissektion werden zusätzlich die Gruppen 12, 13, 14, 15, 110, 111, ev. 16,entfernt.
Im Stadium II und IIIA führt die radikale Lymphknotendissektion zu einer signifikanten Verbesserung des Überlebens bei Patienten mit den Kategorien pN0 und pN1 (UICC). Morbiditäts- und Letalitätsraten sind bei entsprechender Erfahrung des Chirurgen nicht erhöht (German Gastric Cancer Study, National Cancer Centre Tokyo,Memorial Sloan-Kettering Cancer Center New York). Eine radikale Lymphknotendissektion bedeutet die en-bloc Resektion des zu entfernenden Magenabschnittes, der N1 Lymphknoten (perigastrische Lymphknoten 1-6 bei der Gastrektomie, 3-6 bei der subtotalen Gastrektomie), der N2 Lymphknoten ( 7-11 bei der Gastrektomie, 7-9 bei der subtotalen Gastrektomie) sowie der Lymphknotengruppen 12 und 13 der N3 Lymphknoten. Bei entsprechendem Standard der histopathologischen Präparataufarbeitung sind bei einer radikalen Dissektion mehr als 26 entfernte Lymphknoten zu fordern.
| Mediane Überlebenszeit und 5-Jahre Überlebensrate der resezierten Patienten in Abhängigkeit vom UICC-Stadium | ||
| UICC-Stadium | Mediane ÜLZ (Monate) |
5-Jahres Überleben (Prozent) |
| IA | – | 85,2 |
| IB | – | 69,2 |
| II | 40,8 | 43,7 |
| IIIA | 18,9 | 28,6 |
| IIIB | 13,8 | 17,7 |
| IV | 8,4 | 8,7 |
Erweiterte Resektion
Eine Ausdehnung der Resektion (en bloc-Resektion auf Nachbarorgane wie Duodenum, Pankreas, Transversum, Leber) wird bei Tumorinfiltration dieser Organe erforderlich, wenngleich nicht immer zwischen entzündlicher und echter Tumorinfiltration unterschieden werden kann. Cave Tumoreinriß und Inzisionsbiopsie!
Zusammenfassung
Die radikale chirurgische Therapie eines Magenkarzinoms bedeutet für den Betroffenen die einzige Option auf Heilung. Die kurative Resektion umfaßt je nach Lokalisation und Histologie des Tumors die Entfernung desselben im Gesunden oder weit im Gesunden, resultierend in einer subtotalen Gastrektomie, Gastrektomie oder bei Tumorinfiltration von Nachbarorganen oder des distalen Oesophagus in einer Erweiterung des Eingriffs. Im Sinne der Notwendigkeit einer dreidimensionalen Radikalitätserfordernis erfolgt die systematische Lymphknotendissektion der perigastrischen Lymphknoten (N1) und jener entlang der großen versorgenden Gefäße (N2). Die systematische Lymphadenektomie erlaubt nicht nur ein exakteres Staging sondern trägt darüber hinaus zu einer Radikalitätserweiterung und Verbesserung der Therapieergebnisse bei. Der UICC-R0-Resektion kommt bei der Vermeidung eines lokalen Tumorrezidivs die größte Bedeutung zu und kann eigentlich nur dann sicher als solche eingeschätzt werden, wenn die nächst höhere Lymphknotengruppe sicher tumorfrei erscheint. Damit kommt dem Chirurgen eine zentrale prognostische Bedeutung zu. Die Wirksamkeit der radikalen Lymphadenektomie kann heute für die Tumorstadien II und IIIA als gesichert angesehen werden, die Stadien IA, IB und II weisen nach radikaler Lymphadenektomie hervorragende Heilungsergebnisse auf. UICC R1- und R2-Resektionen haben lediglich einen palliativen Charakter mit medianen Überlebenszeiten zwischen 7 und 10 Monaten, ähnlich schlechte Ergebnisse sind für die Tumorstadien IIIB und IV-R0 zu erwarten. Hier versprechen neoadjuvante Therapiemodalitäten für die Zukunft eine Prognoseverbesserung.
