Koordination:
Ch. Sebesta, Wien
Unter Mitarbeit von:
P. H. Clodi, Linz
W. Fortunat, Wolfsberg
W. Hinterberger, Wien
G. Judmaier, Innsbruck
P. Knoflach, Wels
G. J. Krejs, Graz
W. Petritsch, Graz
F. Renner, Ried i. Innkreis
R. Schiessel, Wien
J. Walchshofer, Linz
W. Weiss, Wien
Ziel
Die Endoskopie stellt heute jene Untersuchungsform mit der größten Spezifität und Sensitivität für die Diagnose des Magenkarzinoms dar. Voraussetzung für die hohe Treffsicherheit ist ein standardisiertes Vorgehen im Untersuchungsgang, die obligate Biopsie jeder suspekten Läsion sowie die genaue Lokalisationsangabe verdächtiger Strukturen. Der zusätzliche Einsatz der Endosonographie erweitert den Informationsgehalt der endoskopischen Diagnostik durch Aussagen über die Infiltrationstiefe
Einleitung
Die Ösophagogastroduodenoskopie (ÖGD) ist heute die primäre Untersuchung des oberen GI-Traktes. Die Diagnose Magenkarzinom wird in der Regel endoskopisch gestellt, oder, wo radiologisch vermutet, endoskopisch-bioptisch gesichert. Gegenüber dem Magenröntgen weist die ÖGD nicht nur die Vorteile der wesentlich höheren Sensitivität und Spezifität auf, sondern ermöglicht auch gleichzeitig die Entnahme von Gewebsproben. Darüberhinaus hat seit einigen Jahren die Endosonographie in die Diagnostik Einzug gehalten, mit deren Hilfe das präoperative Staging maligner Tumoren des Gastrointestinaltraktes wesentlich an Exaktheit gewonnen hat.
Makroskopische Diagnostik
Early CancerSeit 1962 wird nach der Definition der Japanischen Gesellschaft für Gastroenterologische Endoskopie zwischen „early gastric cancer“ und fortgeschrittenem Magenkarzinom unterschieden. Der „early cancer“ (=Magenfrühkarzinom) ist definitionsgemäß ein „Karzinom des Magens, dessen Invasion auf Mucosa und Submucosa beschränkt ist, unabhängig vom Vorhandensein oder Fehlen von Lymphknotenmetastasen“ (Kuru 1967). Die Bezeichnung „Magenfrühkarzinom“ bezieht sich also auf das morphologische Bild und das biologische Verhalten des Tumors und nicht auf die Chronologie von Tumorstadien.
Der Beweis für das Vorliegen eines Magenfrühkarzinoms wird durch Resektion im Verein mit Serienschnittuntersuchungen des Resektates erbracht.
| Makroskopisch läßt sich das Frühkarzinom wie folgt unterteilen: | |
| Typ I: | vorgewölbter Typ (protruded type) |
| Typ II: | Oberflächentyp (superficial type) |
| Typ IIa: | erhaben |
| IIb: | flach |
| IIc: | flach eingesenkt |
| Typ III: | ulzerös (excavated type) |
Erfahrungsgemäß macht der Typ IIb (flach) diagnostisch die meisten Probleme, da oft nur Farbveränderungen oder eine angedeutet granuläre Struktur die Läsion anzeigen.
Der Typ IIc wird am häufigsten gefunden. Vorgewölbte Regionen der Mucosa müssen, ebenso wie Ulcera, grundsätzlich biopsiert werden, makroskopisch ist eine Differenzierung gegenüber polypoiden Neubildungen, kompletten Erosionen, Lipidinseln oder Adenomen (borderline lesion) nicht immer sicher möglich.
Die Differentialdiagnose des ulzerösen Typs des Frühkarzinoms ist das benigne Ulcus ventriculi. Auch hier ist eine Unterscheidung nur histologisch bioptisch zu treffen. Aus Gastroskopie und Histologie ergibt sich die Operationsindikation.
Fortgeschrittenes Magenkarzinom
Ein fortgeschrittenes Karzinom liegt vor, wenn der Tumor die Muscularis propria infiltriert hat. Die von Borrmann 1901 erstellte Einteilung ist auch heute noch gültig:
| Typ I: | polypös blumenkohlartige Form |
| Typ II: | exulzerierte Form |
| Typ III: | diffus infiltrierend mit Ulzeratio |
| Typ IV: | diffus infiltrierend (häufig ident mit szirrhösem Karzinom) |
Die Typen I – III nach Borrmann lassen sich meist schon makroskopisch unschwer von gutartigen Läsionen (Polypen, Ulcera) unterscheiden. Diagnostisch macht der Typ IV Schwierigkeiten, da oft nur eine Engstellung der befallenen Magenanteile (Antrum) mit Verminderung oder Fehlen der Peristaltik auffallen. Hier ist die radiologische Diagnostik hilfreich (Kapitel 3). Die Dignität einer makroskopisch verdächtigen Läsion wird histologisch-bioptisch bestimmt, was in der Regel mittels Zangen-Biopsie möglich ist.
 |
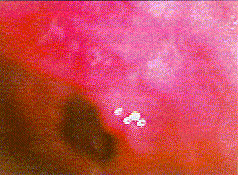 |
| Magenfrühkarzinom: Typ IIa (erhaben). Corpus ventriculi |
Magenfrühkarzinom: Typ IIb (flach). Antrum ventriculi |
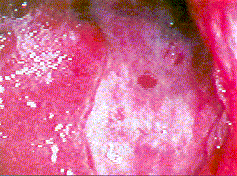 |
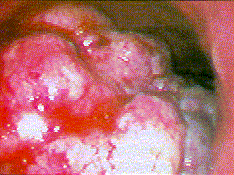 |
| Magenfrühkarzinom: Typ III (ulzerös). Corpus ventriculi |
Magenkarzinom (polypöse Form), Typ I nach Borrmann. Corpus ventriculi |
 |
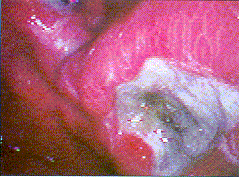 |
| Magenkarzinom (exulzeriert), Typ II nach Borrmann. Angulus ventruculi |
Magenkarzinom (exulzeriert), Typ II nach Borrmann. Subkardial |
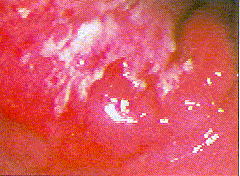 |
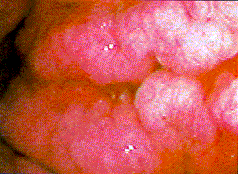 |
| Magenkarzinom (diffus infiltrierend mit Ulzeration), Typ III nach Borrmann: Mittlerer Corpus |
M. Menetrier |
Endoskopisch-Bioptische Diagnostik
Die Indikation zur Biopsie muß heute aufgrund der Frage nach einer eventuellen Helicobacter-pylori-Besiedelung auf nahezu alle Gastroskopien ausgedehnt werden (mindestens zwei Biopsien aus dem Antrum und zwei aus dem Corpus).
Darüberhinaus ist die Biopsie von großer Wichtigkeit bei allen Ulcera, Erosionen, Polypen, atypischen Falten und Riesenfalten, sowie grundsätzlich bei jeder makroskopisch nicht eindeutig benignen Läsion im oberen GI-Trakt.
Für Ulcera gilt, daß je nach Größe der Läsion, zwischen 6 und 12 Biopsien überwiegend vom Ulkusrand (möglichst gesamte Zirkumferenz), aber auch vom Ulkusgrund entnommen werden müssen. Weitere Biopsate erhöhen die Treffsicherheit nicht.
Bei bereits makroskopischem Malignomverdacht sind genaue Lokalisation, sowie Ausdehnung und Abstand des Tumors von der Cardia und vom Pylorus anzugeben (Beurteilung des intraabdominellen Anteiles des Ösophagus bzw. des Magenausganges und des Duodenums), da diese Faktoren, zusammen mit dem histologischen Karzinomtyp (Klassifikation nach Laurén, siehe Kapitel 2 „Pathologie des Magenkarzinoms“), für die Operationsplanung von Bedeutung sind. Negative Histologie bei makroskopisch suspektem Befund muß zu einer baldigen Wiederholung der Endoskopie mit ausgedehnter Probenentnahme und eventueller Schlingenbiopsie Anlaß geben.
Ausdrücklich zu betonen ist, daß die makroskopische Klassifikation aufgrund der mangelnden Bedeutung für die Wahl des weiteren therapeutischen Vorgehens nicht die wichtigste Aufgabe der Gastroskopie ist. Vielmehr müssen folgende Fragestellungen beantwortet werden:
- Ausdehnung des Tumors
- Abstand von der Cardia bzw. vom Pylorus
- Histologische Klassifikation (ausreichende Biopsieanzahl)
Präkanzerosen und endoskopisches Follow up von Läsionen mit erhöhtem Karzinomrisiko im Magen
1. Dysplasie
Dysplastische Areale können sich in Polypen, Ulcera sowie im Niveau der Mucosa finden. Abhängig vom Dysplasiegrad kann folgendes Vorgehen empfohlen werden: bei geringgradiger Dysplasie besteht erfahrungsgemäß eine spontane Rückbildungstendenz. Um sicher zu gehen, daß der Dysplasiegrad nicht zunimmt, ist aber die endoskopisch-bioptische Observanz angezeigt – halbjährliche Kontrollen sind ausreichend. Der Begriff mittelgradige Dysplasie sollte überhaupt nicht mehr verwendet werden, da für diese Kategorie kein klares therapeutisches Vorgehen definiert werden kann.
Der Befund hochgradige Dysplasie muß kurzfristig bestätigt werden und stellt eine Operationsindikation dar, da sich in etwa 75% hieraus ein Karzinom entwickelt. Schließlich muß bei nicht sicher bestimmbarem Dysplasiegrad unverzüglich rebiopsiert werden. Einschränkend ist zu sagen, daß die Dysplasie-Karzinom-Sequenz im Magen nicht so eindeutig nachvollziehbar ist, wie bei Läsionen im Colon. Die Frage nach der Rolle der Dysplasie als „Vorläufer, Mitläufer oder Ausläufer“ eines Magenkarzinoms wird gegenwärtig noch kontroversiell diskutiert.
2. Magenadenome
Magenadenome, die im Gesunden abgetragen wurden (s.u.), sollten nach drei Monaten und in der Folge einmal jährlich nachkontrolliert werden. Nicht sicher im Gesunden entfernte Adenome müssen endoskopisch oder chirurgisch nachreseziert werden. Dies gilt nicht für hyperplasiogene Polypen, die wesentlich häufiger als Adenome gefunden werden und keine Präkanzerose darstellen.
3. Ulcera ventriculi
Die Empfehlung, Ulcera ventriculi bis zu ihrer vollständigen Abheilung endoskopisch-bioptisch zu verfolgen gilt weiterhin, es hat allerdings keinen Sinn, die Intervalle auf weniger als vier Wochen zu verkürzen.
4. Endoskopische Nachsorge im resezierten Magen (nach Ulcus pepticum)
Das Risiko eines Magenstumpfkarzinoms nach Magen(teil-)resektion wird heute geringer eingeschätzt als noch vor wenigen Jahren. Jedenfalls scheint das Karzinomrisiko aber doch in Abhängigkeit vom zeitlichen Abstand zur Operation anzusteigen, sodaß, bis zum Vorliegen neuerer Daten, die Empfehlung der jährlichen ÖGD ab dem 15. postoperativen Jahr aufrecht bleibt. Routinebiopsien von der Anastomose und der kleinen Kurvatur sollten entnommen werden. Für aufgefundene Dysplasieherde im Restmagen gilt im übrigen das unter 1. Gesagte.
Ösophagogastroduodenoskopie mittherapeutischer Zielsetzung
Adenomatöse Polypen können diathermisch abgetragen werden. Wenn histologisch nicht im Gesunden abgetragen wurde und hochgradige Dysplasie nachweisbar ist, kann der Versuch einer endoskopischen Nachresektion unternommen werden. Falls diese nicht möglich ist, muß chirurgisch vorgegangen werden. Auch in Einzelfällen von Magenkarzinom, vor allem bei sehr alten oder multimorbiden Patienten mit stark erhöhtem Operationsrisiko, kann eine endoskopische Therapie sinnvoll und ausreichend sein, wenn das Karzinom lokal umschrieben ist und die Submucosa (Endosonographie) nicht überschritten hat (Frühkarzinome, s.o.). Unter den genannten Voraussetzungen sind die 5-Jahresüberlebensraten nach Operation, denen nach photodynamischer- oder Lasertherapie (Neodym-Yag-Laser), sowie auch jenen nach Schlingenresektion mit vorheriger Unterspritzung gleichwertig.
Screening
Das Ziel jedes Screening-Programmes müßte die vermehrte Diagnosestellung von Frühkarzinomen sein, was gleichbedeutend wäre mit einer Erhöhung der Anzahl von radikal-chirurgisch sanierbaren Fällen, und damit einer Verbesserung der Gesamtprognose. Derzeit existiert weltweit kein kosteneffektives Screening Programm. Allerdings konnte in Japan (wo eine weit höhere Inzidenz an Magenkarzinomen beobachtet wird als in Österreich) durch frühzeitigen Einsatz der ÖGD, z. B. im Vergleich mit den angloamerikanischen Statistiken, eine eindrucksvolle Anhebung der 5-Jahresüberlebensrate beim Magenkarzinom erzielt werden.
Dementsprechend kann, bei weitgehender Verfügbarkeit, geringer Komplikationsrate und niedrigen Kosten, eine großzügige Indikationsstellung für die diagnostische ÖGD empfohlen werden. Besonders gilt dies für die Risikogruppen (Tab. 1), zu denen nach neuestem Stand der Kenntnis auch jüngere Patienten mit chronischer Helicobacter-pylori-assoziierter Antrumgastritis, die intestinale Metaplasien aufweisen, zu zählen sind.
Tab. 1: Risikogruppen, für die ein „Magenkarzinom-Screening“sinnvoll ist:
- Positive Familienanamnese
- Perniziöse Anämie
- Adenome
- M. Menetrier
- Operierter Magen
- Dyspeptische Beschwerden bei Patienten über 50 Jahren
- Helicobacter-pylori-assoziierte Antrumgastritis mit intestinalen Metaplasien bei jungen Patienten
Nach den vorliegenden epidemiologischen Daten dürften 70-80% aller Magenkarzinome auf der Grundlage einer Helicobacter-pylori-Gastritis entstehen. Dadurch könnte sich erstmals die Möglichkeit einer medikamentösen Primärprophylaxe durch Eradikation des Keimes eröffnen. Allgemeingültige Richtlinien für eine Eradikationstherapie in dieser Indikation lassen sich gegenwärtig aber noch nicht ableiten, da gleichaltrige Personen, die kein Magenkarzinom entwickeln, auch in 50-70% Helicobacter pylori-positiv sind.
Komplikationen
Diagnostische Endoskopie
Die Komplikationsrate der Ösophagogastroduodenoskopie liegt bei 0,1%, die Letalität bei 0,005% (Pasricha et al., 1994). Obwohl die Mehrzahl der Komplikationen mit der Sedierung und Prämedikation zusammenhängt (Atemdepression, RR-Abfall, Herzrhythmusstörungen, Aspiration), dürfte die Häufigkeit lebensbedrohender kardialer Komplikationen (Infarkt) durch die Sedierung des Patienten eher vermindert sein. Für die Vorbereitung kommen Tranquillantien (Diazepam, Midazolam), sowie ein Rachenanästhetikum (Xylocainspray) in Betracht. Bei letzterem ist auf eventuelle Allergien zu achten. Sehr selten kommt es bei diagnostischer ÖGD zu Blutung (Ösophagusvarizen, Ulcera, Hämangiome) oder Perforation an Prädilektionsstellen (obere Ösophagusenge, Cardia), sowie im Bereich von Divertikeln, Strikturen, Anastomosen und entzündlich veränderten oder strahlengeschädigten Wandbezirken.
Interventionelle Endoskopie
Deutlich höher liegen die Komplikationsraten bei der therapeutischen ÖGD. Während das Komplikationsrisiko für die Polypektomie nur etwa 1-2% beträgt, kommt es bei palliativen endoskopischen Maßnahmen beim Magenkarzinom in 10-30% zu Komplikationen (siehe: Kapitel 9: „Palliative Therapiemöglichkeiten beim Magenkarzinom“). Beschriebene methodenspezifische Komplikationen bei Thermokoagulation, Lasertherapie und Prothesenimplantationen sind: Blutung, Perforation, Mediastinitis, Sepsis, Prothesendislokation und Trachealkompression. Die höchste Komplikationsrate ist bei Prothesenimplantationen zu erwarten.
Nachsorge
Nach jedem potentiell komplikationsgefährdetem Eingriff im Rahmen einer ÖGD sollte der Patient entweder für 24 Stunden stationär aufgenommen und entsprechend überwacht, oder falls ambulant durchgeführt, instruiert werden, sich bei Auftreten neuer Symptome (z.B. Bauchbeschwerden, Hämatemesis, Melaena) sofort wieder im Spital zu melden
Beurteilungsschwerpunkte der ÖGD (Ösophagogastroduodenoskopie)
- Prograde Beurteilung des gesamten Ösophagus und des ösophagogastralen Überganges
- Magen in prograder Sicht und in Inversion. Angabe, ob ein suffizienter Cardiaschluß beobachtet werden kann. In Inversion Aufsicht auf den Angulus: sog. „Zwei-Höhlenblick“ (Antrum; Corpus-Fundus).
- Bulbus duodeni und Pars descen- dens duodeni. Papillenregion, falls einsehbar
- Bei Beendigung der Untersuchung besonderes Augenmerk auf proxi- males Ösophagusdrittel, das beim Einführen des Gerätes häufig „blind“ passiert wird.
- Aussage über die beobachtete Peristaltik in sämtlichen Abschnitten (bei unklarem Befund – Indikation für das Magenröntgen).
- Histologie, Zytologie, Helicobacterschnelltest.
| Tabelle 2: Tarife Magenröntgen | (Honorar, Unkosten in öS) | |
| Wiener GKK | Magen-Duodenum (Doppelkontrast) |
481,80 607,80 |
| NÖ GKK | Magen-Duodenum (ohne Doppelkontrast) |
884,60 |
| Bgld. GKK | Magen-Duodenum (ohne Doppelkontrast)
Magen-Duodenum |
472,00 1.018,00
526,00 |
| OÖ GKK | Magen-Duodenum (mit Doppelkontrast)
Magen-Duodenum |
665,02
677,32 |
| Ktn. GKK | Magen-Duodenum (mit Doppelkontrast) |
812,00 |
| Sbg.GKK | Magen-Duodenum (mit Doppelkontrast)
Magen-Duodenum |
923,40
951,50 |
| Tir.GKK | Magen-Duodenum plus Magendarmpassage plus Appendix |
226,70 147,60 |
| Vbg.GKK | Magen-Duodenum (mit Doppelkontrast) |
574,00 817,80 |
| Stmk.GKK | Magen-Duodenum (mit Doppelkontrast) |
576,20 506,50 |
| Tab 3: Tarife Gastroskopie | Sonderbestimmungen (Beträge in öS) | |
| Wiener GKK zusätzlich: Regiezuschlag S 360,00 |
554,40 | Ausbildungs- und Gerätenachweis; Einvernehmen ÄK |
| NÖ GKK | 885,00 | keine |
| Bgld.GKK | 757,00 | keine |
| OÖ GKK | 927,50 | Ausbildungs- und Gerätenachweis; Einvernehmen ÄK |
| Ktn.GKK | 830,00 | Endoskopie des oberen Intestinaltraktes, Gastroskopie, Duodenoskopie; keine |
| Sbg.GKK | 770,00 | keine |
| Tir.GKK | 736,70 | nur für Chirurgen 50% der BF |
| Vbg. GKK | 900,00 | Endoskopische Untersuchung der Speiseröhre, des Magens und des Duodenums mit allfälligen Biopsien; keine |
| Stmk.GKK | 750,00 | für Chirurgen und Internisten |
