Koordination:
C. Dittrich, Wien
Unter Mitarbeit von:
H. Hausmaninger, Salzburg
K. Pils, Wien
J. Fiegl, Wien
G. Linemayr, Wien
P. Sevelda, Wien
Problemstellung
Während in früheren Jahren die Zielsetzung einer (mehr oder weniger standardisierten ) Nachsorge nach operiertem Mammakarzinom vorwiegend in der Dokumentation des chirurgisch erreichten Behandlungserfolges und in der Früherkennung von Rezidiven oder Metastasen gesehen wurde, gewannen in letzter Zeit zunehmend Fragen der psychosozialen Betreuung und der Verbesserung der Lebensqualität der operierten Patientinnen an Bedeutung. Daneben sollte nicht außer acht gelassen werden, daß Frauen nach operiertem Mammakarzinom mit einer erhöhten Rate (vor allem metachroner) Zweitneoplasien zu rechnen haben und die Aufgabenbereiche der Nachsorge fließend in solche der Vorsorgemedizin übergehen.
Ziel
Anliegen aller Bemühungen der Nachsorge von Menschen, die an einem Tumor erkrankt sind, ist es, letzteren ein Leben in größtmöglicher medizinischer Sicherheit unter Bedachtnahme aller Risken zu ermöglichen und dabei die Lebensqualität zu maximieren. Durch klare Unterscheidung zwischen unbedingt notwendigen und überflüssigen Untersuchungen und durch Weglassung überflüssiger Einschränkungen der Lebensführung unter gleichzeitiger Betonung der notwendigen soll einerseits das Leben dieser Personengruppe maximiert und optimiert werden und andererseits die vorhandenen Resourcen ökonomisch eingesetzt werden. Dies kann nur durch die jeweils aktuellste Information der betreuenden Kollegenschaft über die neuesten Erkenntnisse auf diesem Gebiet erreicht werden.
Patienteninformation
Ausgangspunkt jeder sinnvollen Tumornachsorge ist eine ausreichende und kompetente Patienteninformation, die der persönlichen Situation der Patientin gerecht wird und für die auch ausreichend Zeit zur Verfügung stehen muß. Die Patienteninformation sollte die folgenden Inhalte berücksichtigen (siehe Tabelle 1):
Tabelle 1: Umfang der Patienteninformation
- Charakteristik der Erkrankung (Hinweis auf fehlende Infektionsgefahr und Erblichkeit)
- Prognose der Erkrankung (mit Betonung günstiger Faktoren)
- Information über Adjuvansmaßnahmen (medikamentöse Tumortherapie, Strahlenbehandlung)
- Ausschaltung von Risikofaktoren (positive Auswirkungen von Nikotinabstinenz und Reduktion des Alkoholkonsums)
- Ernährungsfragen bzw. -empfehlungen (Vermeidung einseitiger Ernährung und sogenannter Krebsdiäten bzw. „Fastenkuren“)
- Lebensstil (Möglichkeit von Auslandsreisen, Impfungen, Sportausübung und normalem Sexualleben)
- Beratung über Kontrazeption oder erwünschte Gravidität (vor allem während oder nach adjuvanter Chemotherapie)
- Evaluation der psychischen Ausgangslage und Angebot psychologischer Hilfestellung, Information über bestehende Selbsthilfegruppen
- Wertung komplementärer Zusatzbehandlungen und Schutz vor Scharlatanerie.
- Beratung bei beruflicher Rehabilitation bzw. hinsichtlich Krankenstand oder Berentung in Zusammenarbeit mit den Sozialdiensten
Adjuvante Therapiemaßnahmen
Im Rahmen einer ausreichenden Patienteninformation werden auch Fragen einer radiotherapeutischen oder medikamentösen Nachbehandlung zu diskutieren sein. Obwohl hier auf Einzelheiten der Indikationsstellung von Radio-, Hormon- oder Chemotherapie nicht eingegangen werden kann, muß betont werden, daß in einer diesbezüglichen Beratung vielfältige Faktoren, wie prä- oder postmenopausaler Status bzw. Alter der Patientin, Lymphknotenstatus (und Zahl befallener Lymphknoten), Rezeptorenbefund, Proliferationskinetik u.v.m. einfließen müssen. Die Komplexizität der heute zur Verfügung stehenden medikamentösen Optionen und die Sequenz der einzelnen Therapieschritte impliziert eine fachlich fundierte Beratung an onkologischen Zentren mit funktionierender interdisziplinärer Kooperation und nach Möglichkeit Behandlung der Patientinnen innerhalb kooperativer Studien.Gerade Patientinnen, die im Rahmen von klinischen Studien (z.B. der Österreichischen kooperativen Studiengruppen) behandelt und betreut werden, werden besser und sorgfältiger nachgesorgt.
Physiotherapie und Rehabilitation
Maßnahmen unmittelbar postoperativ
Bereits am ersten postoperativen Tag soll der Arm der betroffenen Seite so gelagert werden, daß es nicht zur Abflußbehinderung und damit in weiterer Folge zur Entstehung eines Lymphödems kommt. Der Arm kann in einer weichen Schiene oder auf großen Kissen in einer leichten Abduktion und vor allem etwas erhöht liegen. Es ist wichtig, daß weder Verbandmaterial noch Kleidungsstücke den Arm oder die Achsel einengen. Dies ist vor allem dann von Bedeutung, wenn Lymphknoten entfernt wurden. Bereits nach der Entfernung der Drains beginnt die Therapeutin den Arm und das Schultergelenk vorsichtig durchzubewegen, ohne einen Zug auf die Operationswunde auszuüben. Nach und nach wird das passive Durchbewegen durch aktive Bewegungen der Patientin selbst ersetzt. Nach der Nahtentfernung sollten die Halswirbelsäule, beide Schultergelenke und beide Arme frei bewegt werden können.
Prävention von Sekundärschäden
Nach der Entlassung sollte die Physiotherapie noch einige Zeit fortgesetzt werden, denn meist treten Probleme erst zu Hause im Rahmen der Alltagsanforderungen auf. Physiotherapeutin, Ergotherapeutin, Psychologin und Diätassistentin helfen bei der Aufarbeitung der geänderten Situation.
Ein kurzes šbungsprogramm von circa 15 Minuten sollte zunächst unter der Anleitung der Physiotherapeutin erlernt und dann von der Patientin täglich durchgeführt werden. Es beinhaltet šbungen zum Erhalt der freien Schulterbeweglichkeit, šbungen zur Kräftigung von Bauch- und Rückenmuskulatur und Dehnungsübungen, um Fehlbelastungen entgegenzuwirken.Das Tragen von Lasten, oder das lange Herabhängen des „betroffenen“ Armes, aber auch das Tragen einschnürender Kleidungsstücke kann die Entstehung eines Lymphödems begünstigen.
Sportliche Aktivitäten sind prinzipiell erlaubt, wenn sie den Einsatz des „betroffenen Armes“ erfordern (z.B. beim Tennisspielen), jedoch von extremen und insbesondere statischen Belastungen ist strikt abzuraten.
Lange heiße Bäder sind zu vermeiden, da durch die Gefäßweitstellung Stauungen im Bereich der Lymphgefäße begünstigt werden können. Gegen Saunabesuche besteht unter der Voraussetzung, daß die Temperatur nicht zu hoch gewählt, und der Arm der operierten Seite in feuchte, kühle Tücher gehüllt wird, kein Einwand. Das häufig ausgesprochene Verbot von Heilbädern inkl. Moorbädern, des Sonnenbadens, der Bestrahlungsexposition in Solarien entbehrt jeder wissenschaftlich gesicherten Grundlage und sollte nicht weiter ausgesprochen werden.
Physiotherapie bei Funktionsstörungen
Ist nach einem größeren Eingriff die Beweglichkeit des Schultergelenks durch Narbenzüge eingeschränkt, so kann nach abgeschlossener Wundheilung mit einer intensiven Physiotherapie begonnen werden. Ein wesentlicher Bestandteil des Therapiekonzeptes ist die Bewegungstherapie oder Heilgymnastik. Eine Physiotherapeutin kombiniert aktive Bewegungen mit Dehntechniken, um das Bewegungsausmaß des betroffenen Gelenkes zu vergrößern, die Muskulatur zu kräftigen und die Koordination zu verbessern.
Mußte im Rahmen der Operation eine Brust vollständig entfernt werden, so treten neben den oben beschriebenen Beschwerden auch meist Schmerzen im Bereich des Rückens auf. Durch die Asymmetrie kommt es zu einer Fehlbelastung der Brustwirbelsäule und zu einer Veränderung der Muskelzüge, die in einer skoliotischen Fehlhaltung oder einer vermehrten Kyphose resultieren kann. Durch gezielte šbungen können nun die autochtone Rückenmuskulatur und die Bauchmuskulatur gestärkt und vor allem die Haltung korrigiert werden. Dabei ist es wichtig, daß die Patientin die neuerlernten Bewegungsmuster in den Alltag übernehmen kann.
Aus der Vielzahl der passiven therapeutischen Maßnahmen können nur einzelne detaillierter besprochen werden.
Die Manuelle Lymphdrainage (MLD) kann bereits unmittelbar postoperativ begonnen werden. Durch den verbesserten Abtransport von Hämatomresten oder gestauten Sekreten wird die lokale Schwellung reduziert, und damit die Wundheilung gefördert. Aber auch noch später hat die MLD einen positiven Einfluß auf Narbengewebe, indurierte Narben und Verhärtungen des subkutanen Bindegewebes. Diese werden weicher, elastischer und besser verschieblich.
Eine sanfte Streichmassage kann verspannte Muskulatur lockern. Auf feste Knetungen sollte aber verzichtet werden, um die Lymphgefäße nicht zu irritieren.
Ultraschall, eventuell kombiniert mit einem entsprechenden topisch zu applizierenden Medikament (z.B. Contractubex®, Ketosoft®,…), kann zur Lockerung des Narbengewebes eingesetzt werden.
Bestehen Schmerzen im Nacken- und Schulterbereich, empfiehlt es sich, auf mittelfrequente Ströme der Elektrotherapie (z.B. Stereodynator, Wymoton,…) auszuweichen, da die Haut durch diese kaum irritiert wird und die sensible Belastung deutlich geringer als durch die Niederfrequenztherapie ist. Hochfrequenztherapie und alle Applikationsformen der Wärmetherapie sollten wegen der Gefahr des Lymphödems vermieden werden.
Unterwassertherapie kann bei strenger Indikationsstellung unter Beachtung der thermischen Belastung zu einer Erleichterung der Beschwerden führen. Thermalwässer haben wegen der Temperatur meist einen negativen Einfluß auf lokale Schwellungen. Moderate Kryotherapie kann in Kombination mit Heilgymnastik oder allein zur Analgesie eingesetzt werden. Zwischen MLD und Kyrotherapie sollte immer eine Zeitdifferenz von mehreren Stunden eingehalten werden, da beide Therapien unterschiedlichen Effekt auf das Lymphsystem haben und sonst der entstauende Effekt der MLD reduziert würde.
Physiotherapie bei Lymphödem
Kommt es zur Ausbildung eines Lymphödems im Bereich des Armes der betroffenen Seite, so sollte so früh wie möglich mit MLD begonnen werden. Durch die Stimulation zentraler Bahnen und gleichzeitigem Ausstreichen der Peripherie kann sehr rasch eine entstauende Wirkung erzielt werden. Parallel dazu sollte der Patientin ein Kompressionsstrumpf nach Maß angepaßt werden. Dieser Strumpf soll nach Möglichkeit den gesamten Arm inklusive Finger umschließen und über einen Gurt im Schultergürtelbereich fixiert werden. Da das Tragen des Strumpfes meist als stigmatisierend und unangenehm empfunden wird, ist es besonders wichtig, die Patienten über die Möglichkeit der Ausdehnung des Lymphödems und die dadurch entstehende Behinderung aufzuklären.
Um die Entstehung des Lymphödems zu verzögern, sollte der betroffene Arm gelagert werden.
Schmuck, Wäsche und andere Kleidungsstücke dürfen nicht einschneiden, einengen oder Bewegungen verhindern. Im Rahmen der medizinischen Betreuung soll auf den lymphatisch geschwollenen Arm Rücksicht genommen werden. Sowohl Blutdruckmessen als auch Blutabnehmen oder Infundieren stellt eine Irritation des bereits gestörten Lymphsystems dar und sollte daher vermieden werden.
Physiotherapie bei Nervenläsionen
Sowohl durch direkte Tumorumscheidung von peripheren Nerven oder Nervenwurzeln, als auch durch Kompression von Nerven durch das Lymphödem, aber auch als Strahlenspätfolge kann es zu peripheren motorischen und/oder sensiblen Nervenläsionen kommen. Unabhängig von der auslösenden Ursache sind die neurologischen Ausfälle mit nur sehr unbefriedigendem Erfolg durch physiotherapeutische Maßnahmen zu behandeln. Die üblicherweise angewandte Reizstromtherapie wird meist durch die vorgeschädigte Haut schlecht vertragen, und der Erfolg ist durch die Progredienz der Erkrankung gering. Um weitere Gelenksschäden zu vermeiden, können von der Ergotherapeutin Schienen zum Funktionsersatz des betroffenen Nerven und der von ihm versorgten Muskulatur angepaßt werden.
Physiotherapie bei Strahlentherapie
Während der Strahlentherapie soll die Haut durch physiotherapeutische Maßnahmen nicht zusätzlich belastet werden. Lediglich Heilgymnastik und Ergotherapie sollen die Patientin unterstützend begleiten, um der Entstehung von Bewegungseinschränkungen entgegenzuwirken, Schmerzen zu lindern oder die Patientin psychisch zu unterstützen.
Nach Abschluß der Bestrahlungsserie bleibt die Haut meist empfindlich und sollte für längere Zeit nicht durch thermische oder elektrische Reize zusätzlich belastet werden.
Früherkennung von Lokalrezidiv und von Metastasierung
In der Meinung, durch möglichst frühzeitige Erkennung von Lokalrezidiven und von Metastasierung nochmals eine kurative Zielsetzung oder Prognoseverbesserung herbeiführen zu können, wurden vorerst laborintensive und apparativ aufwendige standardisierte Untersuchungsprogramme („Nachsorge-Pässe“) entwickelt, die auf prognostische Faktoren und auf das unterschiedliche Rezidivrisiko sowie Kosten-Nutzen-Analysen bei empfohlenen Untersuchungsprogrammen wenig Bedacht genommen haben. Lediglich bei frühzeitig entdeckten Lokalrezidiven besteht jedoch die potentielle Situation einer sekundären Heilung durch adäquate Maßnahmen.
In den Überlegungen hinsichtlich der Wertigkeit diagnostischer Methoden sollten vor allem Sensitivität und Spezifität einzelner Tests sowie Häufigkeit und Verteilung von Metastasen zum Zeitpunkt der Erstmanifestation Berücksichtigung finden.
In etwa 40 % der Fälle kommt es initial zu einer Aussaat im Skelett, gleich häufig werden viszerale Manifestationen und in etwa 20 % lokoregionäre bzw. Weichteil-Metastasen diagnostiziert.
Lokoregionäre Lymphknoten- und Hautmanifestationen stellen meist kein diagnostisches Problem dar; sie werden im allgemeinen durch Inspektion und Palpation entdeckt. Diverse Laborparameter haben sich bei dieser Metastasenlokalisation als wenig sensitiv erwiesen. Auch die Pleuritis carcinomatosa wird meist klinisch diagnostiziert; 90 % aller Frauen sind zu diesem Zeitpunkt symptomatisch. Die Sensitivität des CEA-Wertes beträgt in dieser Situation etwa 70 %.
Laborparameter zur Diagnostik einer pulmonalen Aussaat sind nur von begrenzter Aussagekraft. Erhöhung der Werte von CEA und LDH weisen eine Sensitivität von 40 % auf. Nur ein Viertel aller Patientinnen mit Lungenmetastasen berichtet über Beschwerden. Auf Thoraxröntgen-Kontrollen kann daher vorerst nicht verzichtet werden.
Hingegen kann eine Lebermetastasierung, die als isoliertes Ereignis nur in 3 -4 % der Fälle in Erscheinung tritt, durch Bestimmung von Gamma-GT (Sensitivität 77 %) bzw. durch die Kombination CEA, GOT und LDH (Sensitivität 91 %) recht gut laborchemisch erfaßt werden. Regelmäßige Ultraschall-Kontrollen bei asymptomatischen Patientinnen mit normalen Laborparametern haben daher keinen gesicherten Stellenwert in der routinemäßigen Nachkontrolle für die Früherfassung von Lebermetastasen.
Patientinnen mit Skelett-Metastasen sind zu 60 -80 % symptomatisch; in 50 -65 % findet sich eine erhöhte alkalische Phosphatase oder ein pathologischer CEA-Wert (Sensitivität 96%), sodaß auf routinemäßig durchgeführte Skelettszintigramme bei beschwerdefreien Patientinnen heute durchaus verzichtet werden kann. Ein radiologisches Skelett-Screening (Sensitivität 50 %) gilt als obsolet und zeichnet sich durch hohen personellen, finanziellen und zeitlichen Aufwand aus. Die Durchführung von Blutsenkung, Elektrophorese, Blutbild und Serumeisen oder -kupfer haben zur Erstdiagnostik von Rezidiven bzw. Generalisation keinen Stellenwert.
Die ursprünglich geäußerte Hoffnung, durch Vorverlegung der Diagnostik der Metastasierung und frühzeitige Einleitung einer Palliativtherapie eine Prognoseverbesserung erreichen zu können, hat sich leider nicht bestätigt. Das šberleben von Patientinnen, deren Wiedererkrankung durch ein „maximal“ Screening-Programm entdeckt wurde, war ident gegenüber solchen, bei denen eine Abklärung erst zum Zeitpunkt von Beschwerden herbeigeführt worden war.
Aufgrund der Beobachtung, daß 60 -80 % der Rezidive und Metastasen innerhalb der ersten 3 Jahre auftreten, werden im allgemeinen in den ersten 2 Jahren drei-monatliche Intervalle, anschließend halbjährliche Kontrollen bis zum 5. Jahr und später jährliche Kontrollen empfohlen (Tabelle 2).
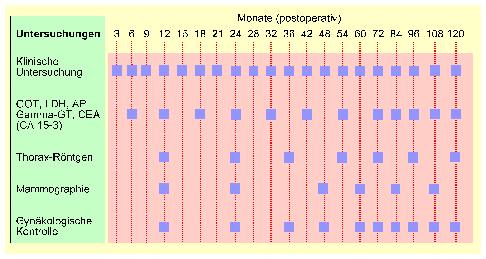
Tabelle 2 Nachsorge von Patientinnen mit Mammakarzinom
Ausgehend von der Tatsache, daß es sich bei Patientinnen mit Mammakarzinom um prognostisch völlig unterschiedliche Gruppen handelt, ist ein risikoadaptiertes Untersuchungsprogramm, das zwischen Low-risk-Patientinnen (Patientinnen mit <4 positiven axillären Lymphknoten, Hormonrezeptor-Positivität, hohem Tumordifferenzierungsgrad, niedrigem Labelling-Index, …) und High-risk Patientinnen (Patientinnen mit >4 (>10) positiven axillären Lymphknoten, Hormonrezeptor-Negativität, niedrigem Tumordifferenzierungsgrad, hohem Labelling-Index, inflammatorischem Karzinom, …) unterscheidet, zu diskutieren.
Beinahe 95 % aller Wiedererkrankungen an Mammakarzinom können aufgrund von Anamnese und genauer klinischer Untersuchung bzw. von serochemischen Untersuchungsmethoden erfaßt werden. Die routinemäßige Erhebung eines sog. „Immunstatus“ bei Frauen nach /mit Mammakarzinom entbehrt jeder wissenschaftlichen Grundlage und ist als überflüssig einzustufen, zumal keine therapeutische Konsequenz erfolgt.
Erfassung von Zweitneoplasien
Neben der Neigung zu Rezidiven und Metastasen haben Patientinnen nach operiertem Mammakarzinom auch ein (gegenüber der Normalbevölkerung) höheres Risiko, an einer Zweit-Neoplasie zu erkranken. Das Risiko für die Entwicklung eines kontralateralen Mammakarzinoms beträgt etwa 1 % pro Patientenjahr und erscheint umso höher, je jünger die Patientin bei der Erst-Operation war bzw. je länger das rezidivfreie Intervall ist.
Bis zu 25 % der länger als 10 Jahre überlebenden Frauen könnten später ein Karzinom in der kontralateralen Mamma entwickeln. Erfreulicherweise konnte dieses Risiko durch eine adjuvante Tamoxifen-Behandlung (20 mg über mehr als 2 Jahre) um ca. 50 % reduziert werden.
In gleicher Häufigkeit können Zweit-Karzinome auch außerhalb der Mamma auftreten, wobei die Ko-Inzidenz zwischen Mammakarzinom und kolorektalen Karzinomen sowie solchen im gynäkologischen Bereich (vor allem Ovarialkarzinomen) bekannt ist. Die Befürchtungen einer erhöhten Rate an Sekundärmalignomen nach adjuvanter Chemotherapie erwiesen sich als unbegründet, neuere Daten sprechen sogar von einem reduzierten Risiko.
Palliative Tumortherapie
Indikationsstellung, Durchführung und šberwachung, vor allem einer medikamentösen (palliativen) Tumortherapie nach aufgetretenen Rezidiven oder Metastasen gehören zu den schwierigsten und verantwortungsvollsten Aufgaben der Nachsorge im weitesten Sinne, da in jedem Einzelfall der mögliche therapeutische Benefit (Palliation) gegen die zu erwartenden und die Lebensqualität belastenden Nebenwirkungen abgewogen werden muß.
Neben kausalen tumortherapeutischen Maßnahmen konnten auch Möglichkeiten der symptomatischen Einflußnahme (adäquate Schmerztherapie, Einsatz von Psychopharmaka, roborierende Maßnahmen, Substitution von Blutbestandteilen, etc.) wesentlich verbessert werden, sodaß Patientinnen auch im Spätstadium ihrer Erkrankung noch ein lebenswertes Leben mit der Erkrankung geboten werden kann.
Schmerztherapie
Ein hoher Prozentsatz an Patientinnen mit Mammakarzinom erleiden Schmerzen im Rahmen des Krankheitsverlaufs.
Diese können entweder unmittelbar tumorbedingt sein, erst durch die Tumortherapie entstehen, Begleiterkrankungen des Tumorleidens darstellen oder unabhängig vom Tumorleiden auftreten. Die differentialdiagnostische Zuordnung stellt die Grundlage für jede rationale Schmerztherapie dar. Es ist zwischen kausalen und symptomatischen Vorgangsweisen zu unterscheiden, wobei bei beiden sowohl lokal- als auch systemtherapeutische Maßnahmen zur Anwendung kommen können. Bei der systemtherapeutischen Analgetikatherapie ist prinzipiell zwischen Analgetikatherapie von akuten und jener von chronischen Schmerzzuständen zu unterscheiden. Während das primäre Ziel der Bekämpfung akut eingetretener Schmerzen deren Linderung ist, ist die Grundlage der chronischen Schmerztherapie die Vermeidung des Auftretens bzw. Wiederauftretens der Schmerzzustände. Dementsprechend hat Analgetikatherapie bei chronischen Schmerzzuständen prophylaktisch, d.h. nach einem fixen Zeitplan, zu erfolgen und nicht -wie häufig immer noch irrtümlich angenommen -bei Bedarf.
Weltweit besteht šbereinkunft, daß Tumorschmerzen im Rahmen eines sogenannten Stufenplans behandelt werden sollen (siehe Tabelle 3). Diese 1986 von der WHO publizierte Empfehlung beinhaltet, daß der Patient zunächst -entsprechend seinen Angaben über die Intensität seines Schmerzes -mit einem der Gruppe der nicht-steroidalen-antiinflammatorischen Therapeutika angehörigen Analgetikum versorgt wird und bei Zunahme des Schmerzes bzw. bei ungenügender Beherrschung dessselben in einer nächsten Stufe ein schwaches Opioid bzw. bei der zu oben vergleichbaren Situation in der darauffolgenden höheren Stufe ein starkes Opioid hinzugefügt werden soll. Diese Schmerztherapie gewährleistet -soferne sie ihrer Intention entsprechend angewandt wird -, daß Patienten einer ihrem Schmerzgrad jeweils entsprechenden suffizienten Behandlung unterzogen werden. Die Zeitdauer, während der die Patienten auf einem jeweiligen Dosislevel behandelt werden, hat sich nach dem Erfolg bzw. Mißerfolg der eingeschlagenen Therapie bzw. nach der Toleranz der Nebenwirkungen zu richten.

Tabelle 3: Stufenplan der medikamentösen
Analgetikatherapie bei Patienten mit Malignomen
(WHO, 1986)
Schmerzen leichter und mittelgradiger Intensität
Leichte und mittelgradige Schmerzen sollen primär mit Paracetamol oder Acetylsalicylsäure oder mit Analgetika vom Typ der nicht-steroidalen-antiinflammatorischen Substanzen versorgt werden, wobei diese bis zum Auftreten limitierender Nebenwirkungen dosiert werden sollen. Bezüglich der Opioide ist zwischen schwächer und stärker wirksamen zu unterscheiden. Schwächer wirksam und damit auch gleichzeitig über geringere Nebenwirkungen verfügend ist die Substanz Tramadol (Tramal®). Durch eine relativ kurze Wirkdauer von nur 4 Stunden ist eine häufigere Einnahme nötig. Um die Compliance der Patienten zu erhöhen, befindet sich eine Retard-Form in Erprobung. In Form von höher dosiertem Dihydro-Codein, welches in eine slow-release Galenik gebracht wurde (Codidol® retard), ist diese Intention bereits verwirklicht und verfügbar.
Schmerzen starker Intensität
Unter den Opioiden mit starker Wirkung, die bei starken Schmerzen einzusetzen sind, ist Morphin der Standard. Die Retard-Form (Mundidol® retard) ermöglicht eine nur 2x tägliche Dosierung. Prinzipiell hat Morphin den Vorteil, daß es, wenn erforderlich, beliebig hoch dosiert werden kann, wobei die Dosierung durch die eintretenden Nebenwirkungen limitiert wird. Während die leicht euphorisierende Wirkung des Morphiums ein durchaus erwünschter Nebeneffekt ist, stellen Müdigkeit, orthostatische Probleme und insbesondere die hartnäckige Obstipation unerwünschte Nebeneffekte dar. An regelmäßige Laxierung ist prophylaktisch zu denken. Die Suchtgefahr ist bei der Behandlung von Malignompatienten ein absolut zu vernachlässigender Faktor. Insbesondere darf Patienten nicht aus Angst vor der Entwicklung einer Arzneimittelabhängigkeit adäquate Analgesie versagt werden. Mit der Gruppe der Bisphosphonate stehen insbesondere in der Situation ossärer Metastasierung äußerst wirkungsvolle kausaltherapeutische, und damit auch analgetisch wirkende Substanzen, wie das Clodronat (Lodronat®, Bonefos®) oder das Pamidronat (Aredia®), zur Verfügung.
Betreuung aus psychoonkologischer Sicht
Patientinnen mit Brustkrebs sind einer mehrfachen psychischen Belastung ausgesetzt: durch die Erkrankung und durch die therapeutischen Maßnahmen (Operation, Chemotherapie, …).
Krisensituationen
Im Laufe der Erkrankung ist die Patientin immer wieder Krisen ausgesetzt (Diagnosemitteilung, Operation, histologischer Befund, adjuvante Therapien, Veränderung des Körperbildes, Rezidiv, usw.). Die Folge ist starke emotionale Spannung, die eine kognitive Einschränkung mit sich bringt. Die eingeschränkte Aufnahmefähigkeit macht daher wiederholte Gespräche notwendig.
Compliance
Die der Sprache der Patientin angepaßte Information über diagnostisches und therapeutisches Procedere wirkt entängstigend und ist die Basis für Compliance. Prinzipielle Gesprächsbereitschaft, soweit vertretbar, über Angebote komplementärer Therapiemethoden stärkt die Vertrauensbasis und verringert das Risiko, daß sich die Patientin fragwürdigen Therapieformen zuwendet.
Soziales Netz
Das Überprüfen sozialer Parameter ist ebenso wichtig wie das Erheben des somatischen Befundes. Wie sieht das soziale Netz der Patientin aus? Wer ist ihr Ansprechpartner zu Hause? Wer kümmert sich um die Patientin?
Angehörige miteinbeziehen
Wann immer dies möglich ist, sollen Angehörige in Gespräche miteinbezogen werden. Es ist wichtig, daß die Information über die Krankheit für Patientin und Angehörige(n) gleichlautet, um deren Gesprächsbasis zu sichern! Gleichrangig mit somatischen Fragen und im Gespräch besonders wichtig ist die Frage nach der psychischen Befindlichkeit. Dazu gehört der Hinweis auf die Möglichkeit psychotherapeutischer Unterstützung zum besseren Umgang mit der Situation und damit zur Verbesserung der Befindlichkeit.
Unterstützung für den Arzt
Das Gespräch mit Krebskranken bedeutet die Konfrontation mit Leid, Tod, Ohnmacht und Angst und gehört für den Arzt zu den belastendsten Situationen. Der Effekt eines Gespräches wird vom Gesprächsklima mitbestimmt. Hilfreiche Unterstützung bieten Weiterbildungsveranstaltungen in ärztlicher Gesprächsführung und Supervision (z.B. Balintgruppen)
Organisation der Tumornachsorge
Tumornachsorge ist ein interdisziplinäres Gebiet, das den gezielten und abgestimmten Einsatz sämtlicher zuvor beschriebener medizinischer Disziplinen bzw. Personengruppen erfordert. Daneben wäre auch eine personelle Aufstockung vorhandener sozialmedizinischer Dienste (Sozialarbeiter) wünschenswert (Beratung bei Umschulung, Berentung, Gebührenbefreiungen, Bereitstellung von Haushalts- und Familienbeihilfen etc.).
Dokumentation
Die Nachsorge dient auch der Qualitätskontrolle der Primärbehandlung. Die statistische Evaluation von Rezidivraten, rezidivfreiem Intervall und šberlebenszeiten in Korrelation mit prognostischen Faktoren und Untergruppen wird erst durch eine gewissenhafte Verlaufskontrolle und Dokumentation ermöglicht.
Zur organisatorischen Erleichterung dieser Aufgabenbereiche wurden in den letzten Jahren auch regionale Krebsregister mit zum Teil unterschiedlicher Zielsetzung geschaffen. Diese Datenbanken dienen als Nachsorgeregister nicht nur zur Erarbeitung von statistischem Material, sondern vor allem auch zur Verbessserung des Informationsflusses zwischen allen mit Tumorpatienten befaßten Ärzten und zur organisatorischen Erleichterung der Nachsorge durch integrierte Einberufungs- und Mahnsysteme.
Empfehlung
Da in Österreich über 30.000 Tumorpatienten jährlich neu erfaßt werden und früher oder später fast zwei Drittel aller Patienten in aktiver Behandlung wegen eines Rezidivs oder einer metastatischen Aussaat stehen, ergibt sich aus diesen Zahlen auch eine quantitative Problematik von Nachsorgekonzepten. Diesbezüglich bestehen in Mitteleuropa unterschiedliche Modelle, die sich nach vorhandenen organisatorischen Strukturen und regionalen Gegebenheiten orientieren. Auf Grund der gegebenen strukturellen und finanziellen Voraussetzungen der ärztlichen Versorgung erscheint die anderweitig bereits praktizierte Vorgangsweise, die Nachsorge an praktizierende Ärzte zu delegieren, in Österreich vorerst nicht denkbar. Wenig zweckmäßig und auch unnotwendig ist hingegen eine rein klinikorientierte Nachsorge unter Ausschaltung des Hausarztes und zum Teil in Form von Doppel- und Dreifach-Untersuchungen an verschiedenen Spitals-Ambulanzen.
Den Wünschen aller Beteiligten kommt ein System alternierender Kontrollen zwischen Hausarzt und Nachsorgestelle als koordinierendem Zentrum entgegen, da dies nicht nur eine finanzielle, sondern auch zeitliche und personelle Entlastung der Spitäler ermöglicht, und auch eine Integration des Hausarztes, der sich in Hinkunft in vermehrtem Ausmaß mit Inhalten und Problemen der Tumornachsorge wird auseinandersetzen müssen. Durch Vermeidung von Überdiagnostik und Übertherapie sollte auch der erschwerten Finanzierbarkeit unseres Gesundheitswesens Rechnung getragen werden.
