Koordination:
H. J. Samec, St. Veit
Unter Mitarbeit von:
A. Gangl, Wien
G. Judmaier, Salzburg
G. J. Krejs, Graz
W. Petritsch, Graz
R. Schöfl, Wien
W. Weiss, Wien
Problemstellung/Ziel
Das kolorektale Karzinom neigt zu einem späten Zeitpunkt des Krankheitszustandes zur Entwicklung von Symptomen. Diese sind eher unspezifisch. Differentialdiagnostisch müssen sehr oft eine Reihe anderer Erkrankungen, wie Divertikulose, Hämorrhoiden, entzündliche Darmerkrankungen, etc., abgeklärt werden. Bei der Diagnosestellung „Karzinom“ stellt die chirurgisch-radikale Resektion zur Zeit die einzig mögliche kurative Therapiemodalität dar. Es sollte daher immer die onkologisch adäquate Resektion angestrebt werden. Die Operationsstrategie muß jedoch vom Zustand des Patienten zum Diagnosezeitpunkt (akut/elektiv) abhängig gemacht werden.
Einleitung
Dem erklärten Ziel jeder Diagnostik, krankhafte Veränderungen in einem möglichst frühen Stadium zu erkennen, kommen die endoskopischen Methoden am nächsten. Durch die direkte Betrachtung von Läsionen und der Möglichkeit durch Biopsien deren Dignität histopathologisch zu erkennen, sind sie allen indirekten Methoden überlegen. Zudem bieten sie auch die Möglichkeit zu direkten therapeutischen Interventionen. Dies gilt ganz besonders für die Koloskopie, einer komplikationsarmen Methode, den gesamten Dickdarm und das terminale Ileum zu untersuchen.
An der Internen Abteilung St. Veit/Glan lag die Komplikationsrate bei 23.000 diagnostischen Koloskopien mit drei Perforationen, davon eine letal, bei 0,016%. Unter den letzten 17.000 Untersuchungen mit den besser ausgereiften neueren Instrumenten kam es zu keinen Komplikationen mehr. Ähnliche aktuelle Zahlen liegen auch aus Ludwigsburg (Frühmorgen) mit einer Komplikationsrate von 0,05% vor. In älteren Literaturangaben, die aber schon über 20 Jahre zurückliegen, sind die Komplikationsraten deutlich höher.
Daher kann die Indikation zur Koloskopie sehr weit gefaßt werden:
Indikationen:
- Jeder Verdacht auf eine Erkrankung des Kolons und des terminalen Ileums
- zur Sicherung der Diagnose bei röntgenologischen Befunden
- für therapeutische Eingriffe (Polypektomie, Blutstillung usw.)
- zur Vorsorge und Früherkennung
- zur Verlaufsbeobachtung und NachsorgeKontraindikationen:Absolute:
Aus all diesen Gründen ist die Koloskopie die Methode der Wahl zur Diagnostik von Tumoren und anderen Erkrankungen des Dickdarms und des terminalen Ileums.
Darüberhinaus gibt uns heute die Endosonographie die Möglichkeit, die Darmwand in ihrem schichtweisen Aufbau darzustellen und intramirale Prozesse in ihrer Ausdehnung sichtbar zu machen sowie Lymphknoten in der unmittelbaren Umgebung nachzuweisen.
Kontraindikationen:
Absolute:
- Mangelnde Kooperation
- Peritonitis
- Hämorrhagische Diathese (Biopsien und Ektomien)
Relative:
- Floride entzündliche Darmerkrankungen
- Ausgeprägte cardiale Insuffizienz
- Ausgeprägte respiratorische Insuffizienz
Makroskopische Diagnostik
Dysplasie – Karzinomsequenz
Die häufigsten Tumore des Dickdarms sind Polypen, das sind Vorwölbungen der Schleimhaut in die Lichtung. Man unterscheidet zwischen nicht-blastomatösen und blastomatösen Polypen, den Adenomen. Eine Differenzierung zwischen den beiden Arten ist makroskopisch nicht möglich. Erst durch die histologische Untersuchung kann zwischen echten Neoplasien und anderen polypoiden Läsionen, den sogenannten „tumor-like-lesions“ unterschieden werden.
Diese Unterscheidung ist unbedingt anzustreben, da davon das weitere Vorgehen abhängt. Denn nur Adenome sind Ausdruck von Dysplasien, die eine Tendenz zur Karzinomentwicklung zeigen.
Dysplasien sind eindeutig neoplastische, nicht-invasive Alterationen des Epithels mit Abweichungen vom Normalbefund in Architektur, Zytologie und Differenzierung.
Man unterscheidet
- leichte
- mittelgradige (mäßige)
- hochgradige (schwere) Dysplasien.
Schwere Dysplasien zeigen alle histologischen und zytologischen Kriterien der Malignität, sind aber auf die Kolonmukosa beschränkt, ohne die Muscularis mucosae zu durchbrechen. Wegen der besonderen Gefäßversorgung im Kolon – Blut- und Lymphgefäße finden sich erst in der Submucosa – können sie nicht metastasieren und werden daher nach Empfehlung der WHO auch nicht als Karzinome bezeichnet.
Dysplasien stellen sich in der weit überwiegenden Mehrzahl als polypoid wachsende Adenome dar, nur selten bleiben sie im Schleimhautniveau, ragen aus diesem nur wenig hervor (doppelte Schleimhautdicke) oder sind ganz flach eingesenkt, sogenannte „flat-adenoma“.
Diese sind dann nur an einer abweichenden Schleimhautfärbung oder gar nicht erkennbar. Gut erkennbar sind sie in einer melanotischen Schleimhaut, da sie kein Melanin aufnehmen und sich daher als blasse Areale von der Umgebung abheben.Unter den Adenomen unterscheidet man nach ihrem histologischen Aufbau (Abb. 1)
- tubuläre
- villöse
- tubolo-villöse
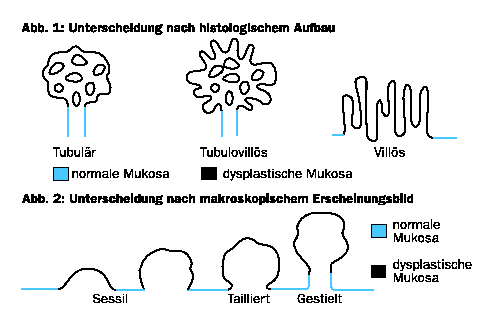
und nach ihrem makroskopischen Erscheinungsbild (Abb. 2)
- gestielte
- taillierte
- sessile.
Nicht alle Adenome entwickeln ein Karzinom. Die Tendenz dazu hängt ab vom makroskopischen Erscheinungsbild, vom histologischen Aufbau, vom Grad der Dysplasie und von der Größe. Je größer der villöse Anteil, je schwerer die Dysplasie und je größer das Adenom, desto ausgeprägter ist die Tendenz zum Übergang in ein Karzinom. Sessile Adenome sind häufig villöse Adenome und neigen öfter zur malignen Entartung mit tieferer Invasion und Lymphknotenmetastasierung.
Darum müssen Adenome immer in toto entfernt und histologisch untersucht werden. Nur so ist es möglich, eine schwere Dysplasie oder ein invasives Karzinom in einem Polypen auszuschließen. Die Entfernung von Adenomen in toto bedeutet sekundäre Krebsprophylaxe. In bestimmten Fällen von Adenomen mit invasivem Karzinom ist die Polypektomie auch eine suffiziente Krebstherapie, wie später noch ausgeführt werden wird.
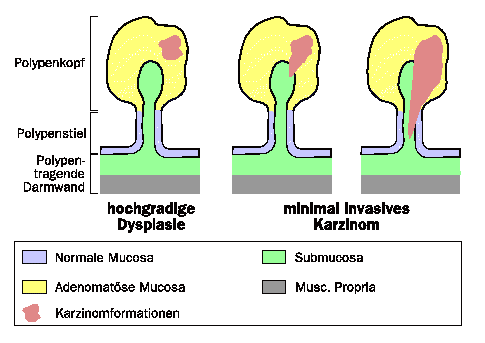
Der erste Schritt hin zum Dickdarmkarzinom nach der Nomenklaturempfehlung der WHO erfolgt mit dem Durchbruch der hochgradigen Dysplasie in die Submucosa.
Damit sind die Voraussetzungen für eine Invasion in Lymph- und Blutgefäße und einer Metastasierung gegeben. Solange das Karzinom auf die Submucosa beschränkt ist und die Muscularis propria freiläßt, handelt es sich um ein sogenanntes Frühkarzinom oder auch minimal invasives Karzinom (alter Begriff „karzinomatöser Polyp“) (Abb. 3).
Diese Karzinome haben eine ausgezeichnete Prognose, sind histologisch oft gut bis mäßig differenziert und zeigen nur in etwa 3% eine regionale Lymphknotenmetastasierung. Nach UICC handelt es sich dabei um ein T-1 Stadium. Bei weitergehender Infiltration kommt es in der Folge zu den verschiedenen T – N – M Stadien nach der UICC-Klassifizierung, die schon in pathologischen Referaten abgehandelt wurden.
Erst beim fortgeschrittenen kolorektalen Karzinom, welches zumeist eindeutig als irreguläre, ulzerierte, brüchige Gewebsläsion imponiert, korreliert der makroskopische Eindruck gut mit dem histologischen Befund.
Bei der endoskopischen Beurteilung von kolorektalen Karzinomen ist zu bedenken, daß im Gegensatz zur makropathologischen Beurteilung eines resezierten Tumors endoskopisch nicht selten nur Teile des Tumors eingesehen werden können (z.B. stenosierender Tumor, Läsion direkt oral einer Flexur/Biegung). Die unterschiedlichen Erscheinungsbilder entsprechen darüber hinaus zumindest teilweise unterschiedlich fortgeschrittenen Tumorstadien. Zu unterscheiden sind das polypöse Karzinom – makroskopisch oft nicht vom Adenom (mit oder ohne Karzinom) zu unterschieden, das häufig schüsselförmig ulzerierte Karzinom-Erscheinungsbild eines relativ spät erkannten Kolonkarzinoms bis hin zum zirkulär stenosierenden Tumor. Wesentlich seltener sind plaqueähnliche (plattenartige), leicht erhabene, flache Tumore, eventuell mit zentraler Einsenkung, und Raritäten (strukturierte Läsionen) bei szirrhös infiltrativen Tumoren („Linitis plastica“ des Kolon).
Interessante neue Beobachtungen werden derzeit laufend zu den Begriffen „flat adenoma“ (kleine tubuläre Adenome, die endoskopisch als geringfügige Erhabenheiten mit geröteter Oberfläche imponieren, teilweise auch mit zentraler Einsenkung), „nicht-polypöses Adenom“, „De Novo Karzinom“ bzw. „Mini-De Novo Karzinom“ (max. Durchmesser 10 mm, Karzinom ohne adenomatöse Elemente, Penetration der Muscularis mucosae), bzw. „kolorektales Frühkarzinom“ mitgeteilt. Ursprünglich von japanischen Autoren beschrieben, jetzt auch in anderen Ländern und auch in Europa vermehrt gesucht und gefunden, sind diese Läsionen noch nicht international einheitlich definiert bzw. biologisch charakterisiert. Sie unterstützen jedenfalls die Theorie der möglichen Karzinomentstehung im Kolon außerhalb der Adenom-Karzinom-Sequenz. Probleme bereiten diese Läsionen u. a. durch die schlechte endoskopische Erkennbarkeit (Verbesserung durch Videoendoskopie?, mehr Erfahrung der Untersucher?, Aufsprühen von Farbstoffen?!), aber auch durch den bei „flat adenomas“ gegenüber polypösen Adenomen hohen Prozentsatz hochgradiger Dysplasien (familiäre Häufung und erhöhtes Kolonkarzinomrisiko bei sog. „Flat adenoma“ Syndrom bereits beschrieben).
Karzinomrisiko und Überwachung bei chronisch-entzündlichen Darmerkrankungen
Neben den lokalen und systemisch entzündlichen Komplikationen kann sich bei einem Teil der Patienten, als wohl schwerwiegendste Komplikation ein Karzinom entwickeln. Das Risiko eines kolorektalen Karzinoms bei Patienten mit chronisch entzündlicher Darmerkrankung ist allerdings individuell sehr verschieden. Entsprechend unterschiedlich wird auch der Wert von Überwachungsprogrammen beurteilt.
Karzinomrisiko und Überwachung bei Patienten mit Colitis ulcerosa
Es ist heute unbestritten, daß die Colitis ulcerosa mit einem erhöhten Risiko für ein kolorektales Karzinom behaftet ist. Die Bedeutung der Risikofaktoren
- kumulative Dauer der Colitis
- Ausdehnung
- Patientenalter bei Diagnosestellung
- Assoziation mit einer primär-sklerosierenden Cholangitis
wird jedoch unterschiedlich bewertet. Das kumulative Risiko ist nach den neueren Studien deutlich geringer als primär angenommen. Es beträgt ca. 7% nach 20 – und ca. 30% nach 35-jähriger Krankheitsdauer und scheint direkt abhängig vom Alter zur Zeit der Diagnosestellung zu sein. Die Bedeutung der Ausdehnung hinsichtlich des Entartungsrisikos wird jedoch nicht einheitlich beurteilt. So fanden einige Autoren die gleiche Inzidenz bei Pankolitis und linksseitiger Kolitis im Gegensatz zu anderen, die eine eindeutige positive Korrelation zwischen Ausdehnung und Entartungsrisiko festgestellt haben. Eine positive Korrelation zwischen einer großen und kleinen „Risikofläche“ scheint jedoch logisch. Ob auch die Anzahl der entzündlichen Schübe eine Rolle spielt, läßt sich auf Grund der vorliegenden Daten nicht beurteilen.
Ziel eines Überwachungsprogrammes ist es, Veränderungen, die auf ein erhöhtes Entartungsrisiko hinweisen, rechtzeitig zu erkennen und so vor Auftreten eines Karzinoms eine Kolektomie zu ermöglichen bzw. bereits aufgetretene Karzinome in einem möglichst frühen Stadium zu diagnostizieren und einer Operation zuzuführen. Im Hinblick auf die teils mangelhaft angelegten Studien existieren derzeit jedoch keine allgemein akzeptierten Empfehlungen bezüglich eines endoskopischen und histologischen Überwachungsprogrammes.
Auf Grund der vorliegenden Daten, Kosten, Arbeitsbelastung und Compliance ergibt sich somit derzeit lediglich folgende Empfehlung
Aufnahme in ein Überwachungsprogramm:
Bei Pancolitis
- nach 15 Jahren Erkrankungsdauer bei Alter < 40 z. Z. der Diagnose
- nach 10 Jahren Erkrankungsdauer bei Alter > 40 z. Z. der DiagnoseBei linksseitiger Colitis
- nach 20 Jahren Erkrankungsdauer bei Alter < 40 z. Z. der Diagnose
- nach 10 Jahren Erkrankungsdauer bei Alter > 40 z. Z. der Diagnose
Patienten mit Rektum- und Sigmabefall sollen wahrscheinlich nicht unterschiedlich zur Krebsvorsorge bei der Allgemeinbevölkerung kontrolliert werden. Patienten mit einer zusätzlichen PSC haben wahrscheinlich ein zusätzliches Risiko und bedürfen eines individuellen Managements. Die Abstände zwischen den Kontrollkoloskopien wird zwischen ein und fünf Jahren angegeben. Eine gewisse Individualität durch Einbeziehung der Risikofaktoren, Histologie und Klinik scheint gerade in diesem Punkt unumgänglich.
Endoskopie und Wertigkeitvon histologischen Befunden
Die Koloskopie bei der Colitis ulcerosa im Rahmen der Karzinomprophylaxe soll in der Remission durchgeführt werden, da die Beurteilung von Dysplasien während eines akuten entzündlichen Schubes erschwert bis unmöglich ist. Unabhängig des Befallmusters sind multiple Stufenbiopsien aus allen Anteilen des Kolons zu entnehmen. Makroskopisch verdächtige Läsionen sind gesondert zu biopsieren. Dysplasien können als Vor-, Mit- oder Ausläufer eines Colitis-assoziierten Karzinoms vorkommen. Bei Auftreten einer durch einen erfahrenen Pathologen diagnostizierten Dysplasie ist eine prophylaktische Kolektomie indiziert. Ausnahmen mit kurzfristigen Kontrollen erscheinen nur vertretbar bei deutlicher Diskrepanz zwischen histologischem Befund und den Riskofaktoren. Eine Differenzierung zwischen low- and high-grade Dysplasien bezüglich des weiteren Managements ist nicht mehr sinnvoll, da bereits
- bei ca. 20% mit low-grade Dysplasien ein Karzinom vorliegt
- Karzinome ohne Zwischenstufe einer High-grade Dysplasie entstehen können
- und ein sampling error umgangen wird.
Karzinomrisiko und Überwachung bei Patienten mit Mb. Crohn
Im Gegensatz zur Colitis ulcerosa wird das allgemein erhöhte Karzinomrisiko beim Mb. Crohn als deutlich geringer angesehen. Karzinome treten meist sehr spät als stenosierender Prozeß zu Tage und finden sich relativ gehäuft im Dünndarm bzw in den tieferen Wandschichten. Hauptrisikofaktoren für das kolorektale Karzinom sind wahrscheinlich Erkrankungsdauer und Ausmaß des Befalles. Hauptrisikofaktoren für ein Karzinom im Dünndarm sind Strikturen, Fisteln, Erkrankungdauer, männliches Geschlecht und im Rahmen einer Bypassoperation ausgeschaltete Darmschlingen. Eine klinische Unterscheidung zwischen Symptomen im Rahmen eines entzündlichen Schubes bzw. einer Komplikation und Symptomen im Rahmen eines Karzinoms ist nicht möglich. Auf Grund vorliegender Daten ist dzt. eine regelmäßige endoskopische Kontrolle zur frühzeitigen Karzinomerkennung bei Patienten mit Mb. Crohn weder gerechtfertigt noch sinnvoll.
Endosonographie
Methodik
Endosonographie (= endoluminaler Ultraschall) ist die Sonographie mit Ultraschallsonden, die in präformierte oder artefizielle Hohlräume des Körpers eingeführt werden.
Im Falle des Colorectums handelt es sich entweder um eine starre kurze Sonde ohne endoskopische Sichtmöglichkeit zur Untersuchung des Rektums und seiner Umgebung oder um ein flexibles Coloskop mit am Ende aufgesetztem Schallkopf zur Untersuchung des gesamten Dick- und Mastdarms; letzteres Prinzip wird auch als endoskopischer Ultraschall (EUS) bezeichnet.
Das meistgenutzte technologische Prinzip ist das des mechanischen Sektorscanners mit Ultraschallfrequenzen zwischen 5 und 12 MHz, wobei höherfrequente Transducer eine bessere Auflösung mit jedoch geringerer Eindringtiefe und damit Sichtfeld verbinden. 7,5 MHz-Transducer, die meistverwendeten Typen, erlauben eine radiäre beurteilbare Darstellung von etwa 7 cm Tiefe. Die Ultraschallebene steht üblicherweise senkrecht zum Schallkopf. Damit wird ein sonographischer Querschnitt der Darmwand abgebildet, der meist einen Vollkreis (360°) umfaßt. Zur optimalen Schalleitung von und zur Darmwand wird ein Ballon um den Schallkopf oder das Darmlumen mit Wasser befüllt. Eine Reihe von Geräten erlaubt endosonographisch gezielte Punktionen.
Die Darmvorbereitung hängt von der Lokalisation der Pathologie ab und entspricht jener einer Koloskopie. Die Untersuchung erfordert keine zusätzliche Sedierung und dauert 5-20 Minuten. Im Falle einer nicht passierbaren Stenose kann der stenosierte Abschnitt mit Endosonographiesonden (Durchmesse 2-3 mm) durch den Instrumentierkanal eines Coloskops untersucht werden; die dabei erzielbare Bildqualität liegt jedoch etwas unter der konventioneller Endosonographiegeräte.
Komplikationen der Endosonographie entsprechen in Art und Häufigkeit jenen der diagnostischen Kolos- bzw. Rektoskopie.
Indikationen
- Staging hinsichtlich T- und N-Kategorie sowie Beziehung zum analen Sphinkter von bereits nachgewiesenen kolorektalen Karzinomen
- Nachweis von Lokalrezidiven an kolorektalen Anastomosen
- Differenzierung von submukösen Tumoren, vaskulären Veränderungen (Varizen) und extrinsischen, imprimierenden Prozessen
- Nachweis und Lokalisation von Abszessen und Fisteln des kleinen Beckens und Perineums und deren Beziehung zur Darmwand und zum Sphinkterapparat
- Differenzierung von chronisch-entzündlichen Darmerkrankungen
- Untersuchung von Uterus und Adnexen, Prostata und Blase (Gynäkologie und Urologie)
Die Kontraindikationen entsprechen jenen der Koloskopie bzw. Rektoskopie.
Staging
Die Möglichkeit endosonographisch die Schichten der Darmwand zu differenzieren, erlaubt die genaue Bestimmung der Ausdehnung eines Prozesses innerhalb der Darmwand, wie das im Falle des kolorektalen Karzinoms von der TNM-Klassifikation gefordert wird.
Die Treffsicherheit der Endosonographie im Staging kolorektaler Karzinome wird für die T-Kategorie mit 85%, für die N-Kategorie mit 79% angegeben. Fernmetastasen sind mit der Methode üblicherwiese nicht nachzuweisen. Die Treffsicherheit der Endosonographie ist relativ unabhängig vom Ausbreitungsgrad des Primärtumors und lokalen Lymphknotenbefalls und übertrifft die Treffsicherheit der Computertomographie.
Anastomosenrezidive werden von der Endosonographie mit hoher Sensitivität (99%), und damit besser als mit jeder anderen Methode erkannt, jedoch beträgt die Spezifität nur ca. 90%.
Während die Methode im präoperativen Staging des Rectumkarzinoms einen festen Platz einnimmt, hat sie sich beim Kolonkarzinom nicht etablieren können, wohl weil hier therapeutische Konsequenzen (stadienabhängige mulimodale Therapiekonzepte) nicht unmittelbar resultieren. Ebenso spielt sie in der Überwachung von Anastomosen nach Darmresektion aus onkologischer Indikation nur bei kolorektalen, nicht jedoch bei kolo-kolischen Anastomosen eine Rolle, da das Lokalrezidiv nur bei ersteren ein substanielles Problem darstellt. Die relativ hohe Rate falsch positiver Befunde (Spezifität 90%) hat eine generelle Einbeziehung in postoperative Überwachungspläne bislang noch verhindert. Vielleicht stellt ein früh postoperativ angefertigter Referenzbefund und der zunehmende Einsatz der endosonographisch gezielten Punktion eine Lösung des Problems in der nahen Zukunft dar.
Koloskopische Polypektomie
Bis vor wenigen Jahren wurde einhellig die Meinung vertreten, daß jeder Polyp im Colon entfernt gehört. Im Laufe der letzen Jahre hat sich von den USA ausgehend insofern ein Stimmungsumschwung abgezeichnet, daß sog. „kleine Polypen“ keine klinische Bedeutung hätten und demgemäß auch nicht zu entfernen seien. Die jeweilige obere Grenze der vernachlässigbaren Polypen wird unterschiedlich mit 5, 7, und 10 mm angegeben. Wir können diesen Forderungen aus mehreren Gründen nicht zustimmen: Auch bei Polypen, die kleiner als 5 mm sind, wurden in knapp mehr als 3% schwere Zellatypien festgestellt. Weiters wissen wir wenig darüber, wie rasch aus diesen sog. „kleinen Polypen“ größere entstehen. Und schließlich wiesen mehrere Arbeiten darauf hin, daß die Größenschätzung durch den Endoskopiker eine extrem unverläßliche Aussage darstellt, wobei übereinstimmend festgestellt wurde, daß Endoskopiker die Polypen für kleiner halten, als sie tatsächlich sind.Die richtige Plazierung der Schlinge, die Feinregulierung der Energiequelle sowie die gewählte Zeitdauer der Koagulation bestimmen den Erfolg der koloskopischen Polypektomie. Weiters ist darauf zu achten, daß der angeschlungene Polyp nirgendwo die Darmwand berührt. Besonders dicke Stellen können vor der Polypektomie sklerosiert werden. Eine Dopplersonographie vor geplanter Polypektomie wurde bei dieser Polypenform ebenfalls als hilfreich erachtet, hat jedoch noch keine breite Anwendung gefunden. Aus der Sicht des beurteilenden Pathologen sollte die polypöse Läsion möglichst in einem Stück abgetragen werden.
Polypen die kleiner als 5 mm sind, sollten mit der HOT-Biopsiezange abgetragen werden. Die richtige Anwendung dieser Zange ist aber besonders im rechten Kolon wichtig, weil dort gehäuft Blutungskomplikationen bei unsachgemäßer Anwendung beschrieben wurden.
Breitflächige ausgedehnte Polypen können zunächst in mehreren Teilen abgetragen werden. Um das Perforationsrisiko geringer zu halten und gleichzeitig auch den Zugang zu flachen Polyprasen zu erleichtern, ist eine Unterspritzung der Submucosa mit physiologischer Kochsalzlösung vor Polypektomie mit Erfolg zur Anwendung gekommen. Verbliebene Polypenreste kann man mittels Neodym-Yag-Laser sehr effektiv nachbehandeln. Der Laser eignet sich gleichzeitig auch zur palliativen Karzinomtherapie.
Bei Polyposen des Kolons (mehr als 100 Polypen) sollten zumindest fünf Polypen abgetragen und zur histologischen Beurteilung weitergereicht werden.
In den letzten Jahren haben sogenannte flache Adenome vermehrt Beachtung gefunden. Sie sind häufig nur wenige Millimeter groß, von flacher Beschaffenheit mit zentraler Delle, bevorzugt im proximalen Kolon anzutreffen und enthalten schwere Dysplasien. Wenn mehrere Polypen im Kolon ascendens abgetragen werden müssen, dann muß nicht zur Bergung jedesmal das Gerät aus dem Kolon entfernt werden, sondern man kann mehrere abgetragene Polypen mit Hilfe eines Sammelnetzes bergen. Besonders wichtig ist es, bei distal gelegenen stenosierenden Karzinomen auf die rechtzeitige Inspektion des übrigen Kolons nicht zu vergessen: Spätestens intraoperativ sollte diese ergänzende Untersuchung vorgenommen werden. Trägt man bereits makroskopisch suspekte Polypen ab, so empfiehlt es sich, die Abtragungsstelle mit einem Farbstoff zu markieren um bei einer notwendig gewordenen anschließenden Operation die Abtragungsstelle zweifelsfrei auffinden zu können.
Immer wieder wird die Frage diskutiert, in welchen Situationen die endoskopische Entfernung eines malignen Polypen eine ausreichende Therapie darstellt. Sind die schweren Zelldysplasien auf die Lamina propria der Mucosa beschränkt, dann ist die koloskopische Polypektomie mit Sicherheit eine ausreichende Therapie. Erst wenn die Submucosa befallen ist, besteht grundsätzlich ein Metastasierungsrisiko. Es wird in der Literatur mit etwa 5% angegeben und muß gegen die Operationsmortalität elektiver Operationen von bis zu 2% abgewogen werden. Um diese Entscheidung zu treffen, benötigen wir einerseits konkrete Informationen des Pathologen: Ist die Muscularis propria eindeutig nicht infiltriert, ist die Resektionsfläche tumorfrei, finden sich keine Lymph- und Blutgefäßeinbrüche und handelt es sich nicht um ein high-grade-Karzinom, so ist die Polypektomie als ausreichende Therapie zu betrachten. Andererseits wird man bei jungen Individuen das Metastasierungsrisiko von immerhin 5% in Operationsüberlegungen mit einbeziehen müssen.
In großen Sammelstatistiken wird das Risiko der Perforation nach kolokopischer Polypektomie mit etwa 0,3% und das der Blutung bis 1-2% angegeben. Es muß jedoch keineswegs jede Komplikation operativ saniert werden. Manche Autoren empfehlen sogar bei Perforation nach koloskopischer Polypektomie ein konservatives Zuwarten bei Nahrungskarenz und Antibiotikatherapie.
Nachblutungen nach Polypektomien sind auf vielfältige Weise mit endoskopischen Mitteln stillbar:neuerliches Fassen des Stiels und Kompression über mehrere Minuten, Injektionstherapie, Laser sowie das Setzen von Clips. Manche Autoren erwähnen auch den zusätzlichen Einsatz eines pädiatrischen Endoskops zur Stillung von Blutungen. Blutungen nach Polypektomien können bis zu 14 Tage nach dem Engriff auftreten. Es ist daher wichtig, den Patienten über diese Möglichkeit zu informieren und mit entsprechenden Verhaltensmaßregeln zu versorgen. Die Einnahme von Aspirin® erhöht das Risiko einer Blutung.
Arbeiten aus den letzten Jahren zeigen, daß der Abstand erforderlicher Kontrolluntersuchungen nach Polypektomie wesentlich großzügiger gehandhabt werden kann, als man das bisher vermutet hat. Manche Autoren meinen, daß man bis zu 10 Jahren nach einem polypfreien Kolon mit der Kontrolluntersuchung zuwarten könne. Dies gilt sicherlich nicht für Patienten, bei denen ein maligner Polyp endoskopisch abgetragen wurde. Hier sollten bereits nach einem Monat, bzw. nach sechs Monaten Kontrolluntersuchungen durchgeführt werden. Eine jährliche Observanz empfehlen wir für Patienten, bei denen mehr als fünf Adenome abgetragen worden sind.
Aus den widersprüchlichen Daten und Empfehlungen in der Literatur der letzten Jahre empfehlen wir generell folgende Vorgangsweise:
- Erste Kontrolle nach Polypektomie nach einem Jahr,
- bei negativem Ergebnis die nächste Kontrolluntersuchung nach fünf Jahren.
Zusammenfassung
Die Koloskopie ist heute die effektivste Methode in der Diagnostik des kolorektalen Karzinoms. Neuerdings besteht mit der Endosonographie auch die Möglichkeit, ein praeoperatives Staging durchzuführen. Aufgrund ihrer hohen Treffsicherheit stellt die Endosonographie heute die Methode der Wahl zum lokalen Saging (T- und N-Kategorie) des Rektumkarzinoms dar. Die postoperative endosonographische Überwachung kolorektaler Anastomosen kann trotz hoher Sensitivität für Lokalrezidive wegen mangelnder Spezifität noch nicht generell empfohlen werden. Gleichzeitig kann durch die endoskopische Entfernung von Adenomen eine sekundäre Krebsprophylaxe durchgeführt werden und in bestimmten Fällen eines mikroinvasiven Karzinoms eine suffiziente Krebstherapie.Die Komplikationsraten sowohl der diagnostischen als auch der therapeutischen Endoskopie liegen sehr niedrig, daher können die Indikationen sehr weit gefaßt werden.Die Heilungschancen des kolorektalen Karzinoms hängen vom Stadium bei der Operation ab. Da gerade das kolorektale Karzinom in seinem frühen Stadium eine ausgezeichnete Prognose hat, ist unbedingt eine frühe Diagnose anzustreben. Dazu gibt die Österreichische Gesellschaft für Gastroenterologie und Hepatologie für Personen ohne Hinweis auf ein familiäres Risiko folgende Empfehlungen heraus: Personen ab dem 40. Lebensjahr ist in der Vorsorgeuntersuchung die jährliche Untersuchung des Stuhles auf occultes Blut zu empfehlen. Da eine sichere Früherkennung des Kolonkarzinoms nur endoskopisch möglich ist, wird ab dem 50. Lebensjahr alle 5-10 Jahre eine endoskopische Dickdarmuntersuchung empfohlen.
